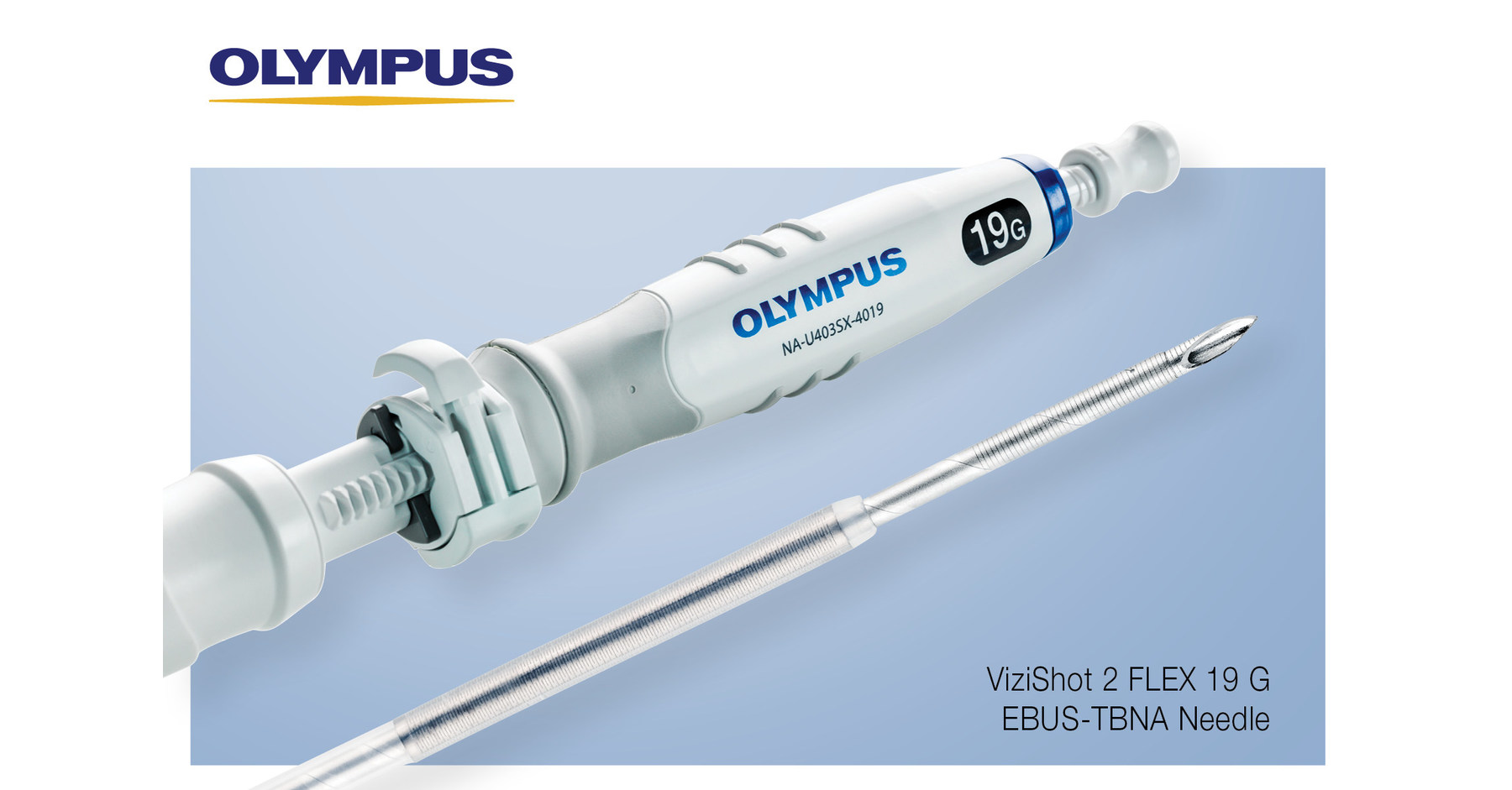
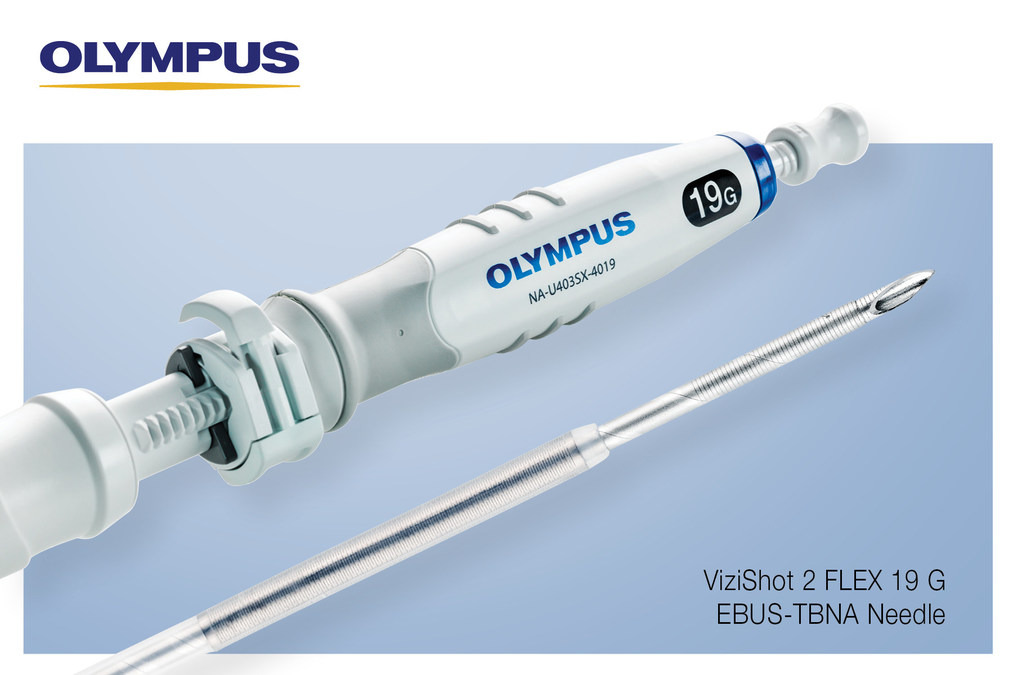
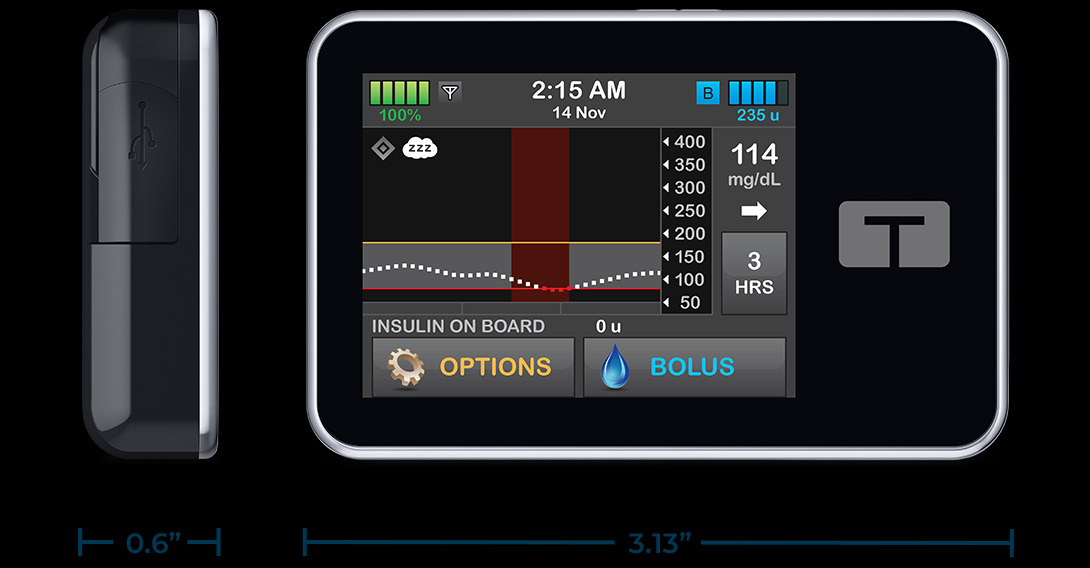
出于安全和性能方面的考虑,Max Mobility/Permobil自愿扩大了对SpeedControl Dial的召回范围,SpeedControl Dial是SmartDrive MX2+助力设备的有线控制选项。该自愿行动适用于在2022年4月25日至2025年7月8日之间生产和分销的所有SpeedControl表盘。受影响的设备已在美国分发。
与现有/先前召回的关系:第一类召回(Z-1116-2025、Z-1117-2025),RES #96086最初于2024年12月20日启动,旨在解决在2023年8月17日至2024年11月21日之间生产和分销的SpeedControl Dials中的印刷电路板组件(PCBA)发生的重大变化。此次召回范围后来扩大到2025年3月28日,涵盖了2023年8月17日至2025年3月10日期间生产和分销的所有产品。Max Mobility/Permobil 收到了 781 起与 PCBA 设计相关的投诉。在这些投诉中,五(5)起因严重受伤,涉及骨折或骨折以及脑震荡。
受影响的产品:所有 SpeedControl 拨盘都受此问题的影响。与 SpeedControl 拨盘相关的特定部件号如下所示:
零件号:
1) MX2-3DCK
2) MX2-3DC
3) MX2-3DCMC
扩大自愿现场移除的原因:通过持续的投诉监测和随后的调查,Max Mobility/Permobil发现了SpeedControl Dial的设计问题,该问题可能导致SmartDrive MX2+发动机出现意外行为。自2022年4月SpeedControl Dial首次投放市场以来,该设计问题一直是SpeedControl拨盘的一部分,并影响到2022年4月25日至2025年7月8日之间生产和分销的所有SpeedControl拨盘,如果SpeedControl Dial和SmartDrive MX2+电机之间出现间歇性的电气连接,则可能会出现以下性能问题:
-继续驾驶:向内按下 SpeedControl 拨盘时,SmartDrive MX2+ 助力设备无法完全停止。
-非自愿移动:意外激活 当拨盘处于零位置且待机模式下拨号灯闪烁时,SmartDrive MX2+ 电机没有用户故意输入 SpeedControl 拨盘。
Max Mobility/Permobil已经确定了54起可能与此问题相关的投诉。在这些投诉中,两(2)起涉及与骨折有关的严重伤害。
健康风险:如果个人使用Max…
更多