Recall notice
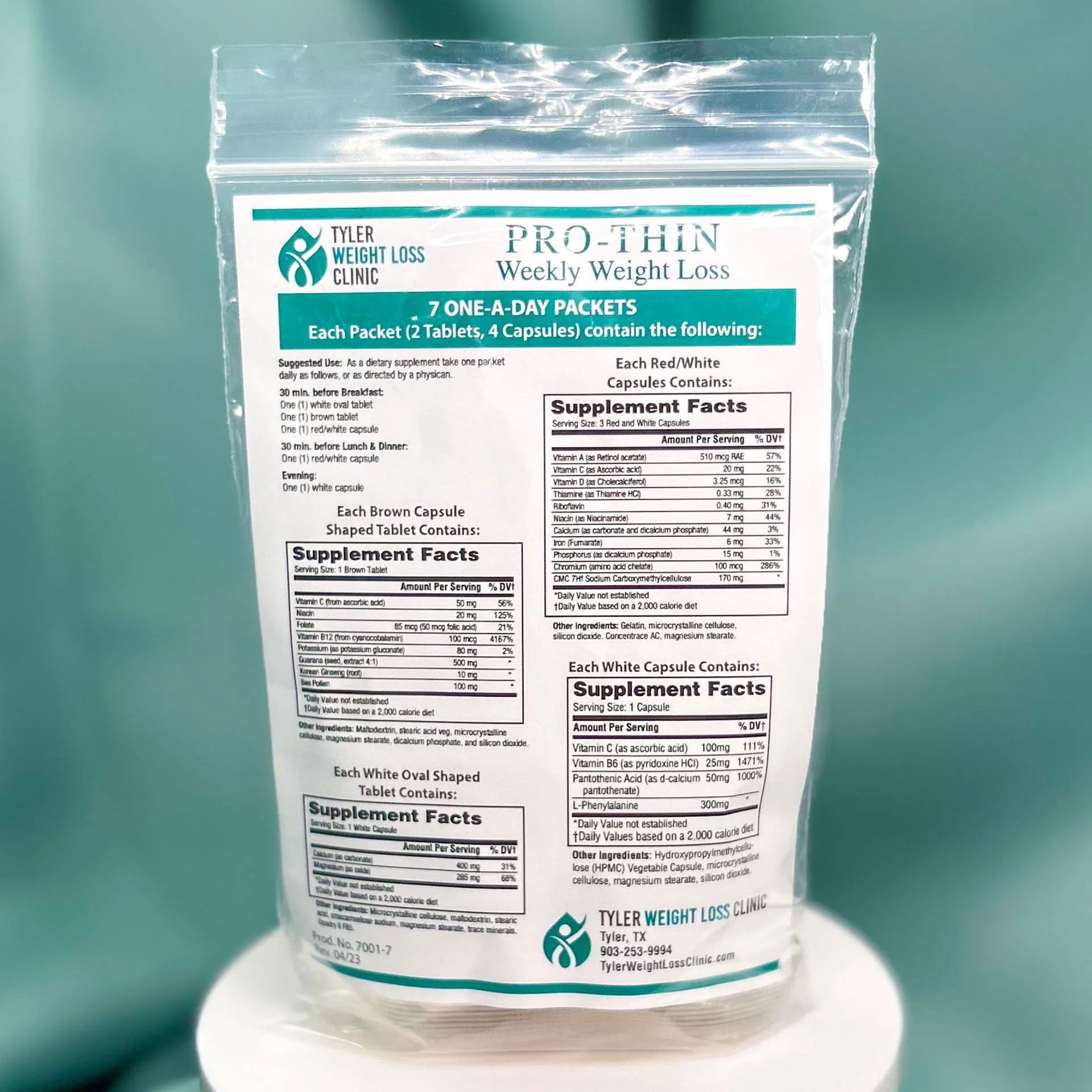
Dwater ruft MyBladder Supplement zur Blasenunterstützung zurück, das aufgrund von E. coli zurückgerufen wurde, USA
vor 4 Monaten •source fda.gov • einzelheiten
Der Rückruf wurde als Klasse II eingestuft.
Quelle: www.accessdata.fda.gov/scripts/ires/index.cfm
28. Oktober 2025:
Purity Products kündigt den Rückruf einer Charge seines Nahrungsergänzungsmittels MyBladder an, da es möglicherweise mit Escherichia coli O7:K1 und 1303 kontaminiert ist. MyBladder wurde in den USA per Direktlieferung an Verbraucher…