Recall notice
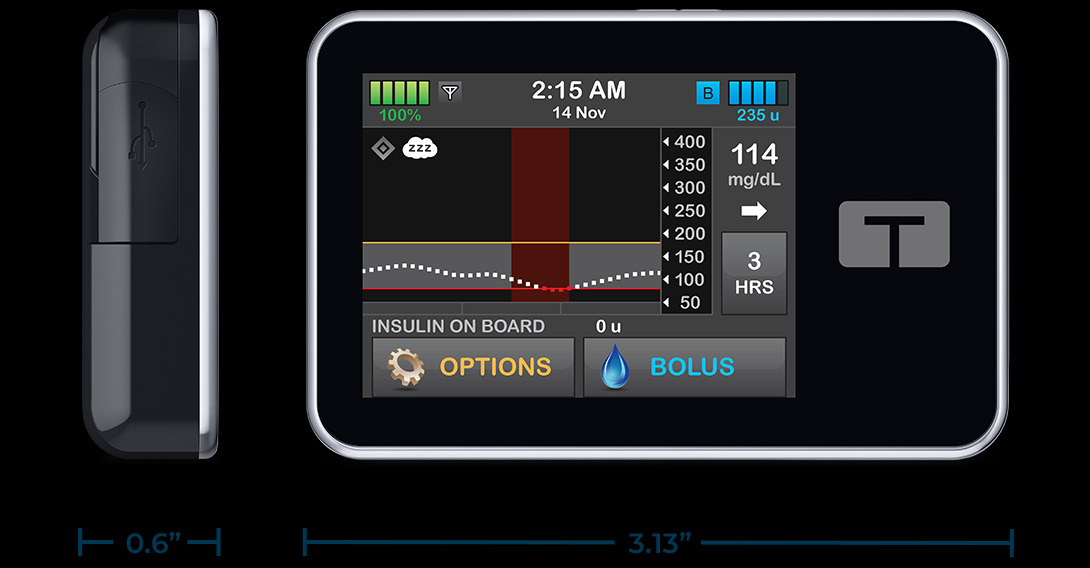
t:slim X2 Insulinpumpen aufgrund einer Fehlfunktion des Geräts zurückgerufen, USA
vor 7 Monaten •source fda.gov
United States
Tandem Diabetes Care, Inc. (Nasdaq: TNDM) hat eine freiwillige Korrektur durch medizinische Geräte für ausgewählte T:slim X2 Insulinpumpen angekündigt, um ein potenzielles Lautsprecherproblem zu beheben, das einen Fehler auslösen kann, der zur Unterbrechung der Insulinabgabe führen kann. Es gab 700 bestätigte Nebenwirkungen, definiert als bestätigter hoher Blutzucker und/oder ein Ereignis, das eine medizinische Intervention erfordert, und 59 gemeldete Verletzungen. Es wurden keine Todesfälle gemeldet. Die betroffenen Geräte wurden in den USA vertrieben.Der Fehler, der dem Benutzer als Störungsmeldung 16 angezeigt wird, stoppt die Insulinabgabe und beendet die Kommunikation zwischen der Insulinpumpe und dem Gerät zur kontinuierlichen Glukoseüberwachung (CGM). Wenn nichts dagegen unternommen wird, könnte dies zu einer Hyperglykämie führen, da die Insulinabgabe unterbrochen wird, die CGM-Glukosewerte in Echtzeit geschätzt werden und die CGM-Trends angezeigt werden. In schweren Fällen von Hyperglykämie kann der Benutzer einen Krankenhausaufenthalt oder eine Intervention durch einen Arzt benötigen.
Weitere Informationen, einschließlich einer durchsuchbaren Liste mit Seriennummern der betroffenen Pumpen, finden Sie unter tandemdiabetes.com/mal16-2025.
Tandem wird ein Software-Update veröffentlichen, das die Früherkennung von Lautsprecherausfällen verbessern soll. Mit diesem Update werden auch anhaltende Vibrationsalarme eingeführt, um potenzielle Sicherheitsrisiken zu verringern. Tandem benachrichtigt alle Pumpenbenutzer, wenn das Software-Update verfügbar ist, und fordert die Pumpenbenutzer auf, das Update ihrer Insulinpumpe abzuschließen.
Wichtige Sicherheitsinformationen: NUR RX. Die t:slim X2-Pumpe mit interoperabler Technologie (die Pumpe) und Control-IQ+ Technologie (Control-IQ+) ist für den Gebrauch durch einen einzelnen Patienten vorgesehen. Die Pumpe und Control-IQ+ sind für die Anwendung mit NovoLog- oder Humalog U-100-Insulin indiziert. t:slim X2 Insulinpumpe: Die Pumpe ist für die subkutane Verabreichung von Insulin in festgelegten und variablen Raten zur Behandlung von Diabetes mellitus bei Personen vorgesehen, die Insulin benötigen. Die Pumpe ist in der Lage, zuverlässig und sicher mit kompatiblen, digital verbundenen Geräten, einschließlich automatisierter Insulindosierungssoftware, zu kommunizieren, um Folgendes zu empfangen, auszuführen und bestätige Befehle von diesen Geräten. Die Pumpe ist für Personen ab 2 Jahren geeignet. Control-IQ+-Technologie: Die Control-IQ+-Technologie ist für die Verwendung mit kompatiblen integrierten kontinuierlichen Glukosemessgeräten (iCGM, separat erhältlich) und alternativen Controller-Pumpen (ACE) vorgesehen, um die Abgabe von Basalinsulin auf der Grundlage von iCGM-Werten und vorhergesagten Glukosewerten automatisch zu erhöhen, zu verringern und auszusetzen. Es kann auch Korrekturboli ausgeben, wenn der Glukosewert voraussichtlich einen vordefinierten Schwellenwert überschreitet. Die Control-IQ+ Technologie ist für die Behandlung von Typ-1-Diabetes mellitus bei Personen ab 2 Jahren und von Typ-2-Diabetes mellitus bei Personen ab 18 Jahren vorgesehen.
WARNUNG: Control-IQ+ darf nicht bei Personen unter 2 Jahren mit Typ-1-Diabetes oder unter 18 Jahren mit Typ-2-Diabetes angewendet werden. Es sollte auch nicht bei Patienten angewendet werden, die weniger als eine tägliche Gesamtinsulindosis von 5 Einheiten Insulin pro Tag benötigen oder die weniger als 20 Pfund (9 Kilogramm) wiegen, da dies die erforderlichen Mindestwerte sind, die für den sicheren Betrieb von Control-IQ+ erforderlich sind.
Benutzer der Pumpe und Control-IQ+ müssen: die Insulinpumpe, iCGM und alle anderen Systemkomponenten gemäß ihren jeweiligen Gebrauchsanweisungen verwenden. Die Nichtbeachtung dieser Anwendungshinweise kann zu einer Über- oder Unterabgabe von Insulin führen. Dies kann zu Hypoglykämie (niedriger BG) oder Hyperglykämie (hoher BG) führen.
Quelle: www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/tandem-diabetes-care-issues-voluntary-medical-device-correction-select-tslim-x2-insulin-pumps
Bemerkungen
Kommentar