Recall notice
Rappel de pompes à insuline t:slim X2 en raison d'un dysfonctionnement de l'appareil, USA
il y a 7 mois •source fda.gov
United States
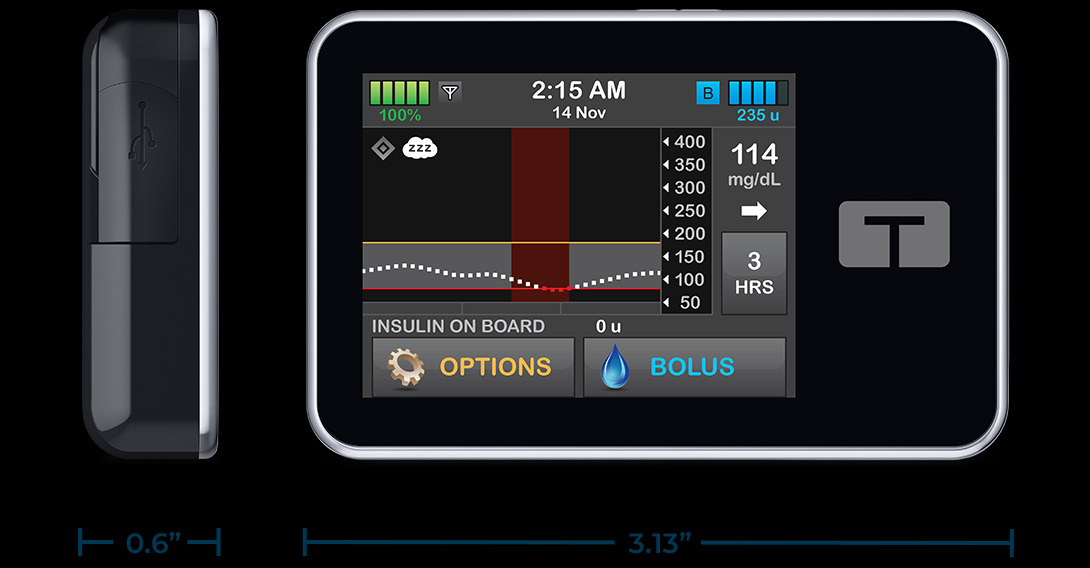
Tandem Diabetes Care, Inc. (Nasdaq : TNDM) a annoncé une correction volontaire du dispositif médical pour certaines pompes à insuline t:slim X2 afin de résoudre un problème potentiel lié au haut-parleur qui peut provoquer une erreur entraînant l'arrêt de l'administration d'insuline. 700 effets indésirables confirmés, définis comme une hyperglycémie confirmée et/ou un événement nécessitant une intervention médicale, ont été signalés, et 59 blessures ont été signalées. Aucun décès n'a été signalé. Les appareils concernés ont été distribués aux États-Unis.L'erreur, qui apparaît comme une alarme de dysfonctionnement 16 pour l'utilisateur, interrompt l'administration d'insuline et interrompt la communication entre la pompe à insuline et le dispositif de surveillance continue de la glycémie (CGM). Si rien n'est fait, cela pourrait entraîner une hyperglycémie due à l'arrêt de l'administration d'insuline, aux valeurs estimées de la glycémie en temps réel et aux tendances du CGM. Dans les cas graves d'hyperglycémie, l'utilisateur peut nécessiter une hospitalisation ou l'intervention d'un professionnel de santé.
De plus amples informations, y compris une liste consultable des numéros de série des pompes touchées, sont disponibles sur tandemdiabetes.com/mal16-2025.
Tandem publiera une mise à jour logicielle conçue pour améliorer la détection précoce des défaillances des haut-parleurs. Cette mise à jour introduira également des alertes de vibrations persistantes afin de réduire les risques potentiels pour la sécurité. Tandem informera tous les utilisateurs de pompes lorsque la mise à jour logicielle sera disponible et leur demandera de terminer la mise à jour de leur pompe à insuline.
Informations de sécurité importantes : RX UNIQUEMENT. La pompe t:slim X2 dotée de la technologie interopérable (la pompe) et de la technologie Control-IQ+ (Control-IQ+) est destinée à être utilisée par un seul patient. La pompe et Control-IQ+ sont indiqués pour être utilisés avec l'insuline NovoLog ou Humalog U-100. Pompe à insuline t:slim X2 : La pompe est destinée à l'administration sous-cutanée d'insuline, à des doses fixes et variables, pour la prise en charge du diabète sucré chez les personnes nécessitant de l'insuline. La pompe est capable de communiquer de manière fiable et sécurisée avec des appareils compatibles connectés numériquement, y compris un logiciel de dosage automatique de l'insuline, pour recevoir, exécuter et confirmez les commandes de ces appareils. La pompe est indiquée pour une utilisation chez les personnes âgées de 2 ans et plus. Technologie Control-IQ+ : La technologie Control-IQ+ est destinée à être utilisée avec des glucomètres intégrés en continu compatibles (iCGM, vendus séparément) et des pompes à commande alternative (ACE) pour augmenter, diminuer et suspendre automatiquement l'administration d'insuline basale en fonction des lectures de l'iCGM et des valeurs de glucose prévues. Il peut également délivrer des bolus de correction lorsque la valeur de glucose devrait dépasser un seuil prédéfini. La technologie Control-IQ+ est destinée à la prise en charge du diabète de type 1 chez les personnes âgées de 2 ans et plus et du diabète de type 2 chez les personnes âgées de 18 ans et plus.
AVERTISSEMENT : Control-IQ+ ne doit pas être utilisé chez les personnes âgées de moins de 2 ans atteintes de diabète de type 1 ou de moins de 18 ans atteintes de diabète de type 2. Il ne doit pas non plus être utilisé chez les patients qui ont besoin d'une dose quotidienne totale d'insuline inférieure à 5 unités d'insuline par jour ou qui pèsent moins de 20 livres (9 kilogrammes), car ce sont les valeurs minimales requises pour que Control-IQ+ fonctionne en toute sécurité.
Les utilisateurs de la pompe et de Control-IQ+ doivent : utiliser la pompe à insuline, l'iCGM et tous les autres composants du système conformément à leurs instructions d'utilisation respectives. Le non-respect de ces instructions d'utilisation peut entraîner une suradministration ou une sous-administration d'insuline. Cela peut provoquer des épisodes d'hypoglycémie (faible taux de glycémie) ou d'hyperglycémie (taux élevé de glycémie).
Une source : www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/tandem-diabetes-care-issues-voluntary-medical-device-correction-select-tslim-x2-insulin-pumps
Commentaires
Commentaire