Recall notice
Dexased™ 和 Dexmedvet™ 盐酸盐注射剂因颗粒物被召回, USA
11 个月前 •source fda.gov
United States
CRONUS PHARMA LLC代表印度海得拉巴的Cronus Pharma Specialties宣布自愿召回,涉及一批包含两个不同批次的产品:Dexased™(Aspen)和Dexmedvet™(Cronus Pharma LLC)。两种产品均含盐酸右美托咪定注射液 0.5 mg/mL,这是美国的一种处方产品,用作狗和猫的镇静剂和镇痛剂,用于促进临床检查、临床手术、小型外科手术和小型牙科手术。该产品还可用作狗和猫的全身麻醉的预麻醉剂。此次召回是作为预防措施进行的,因为在溶液中观察到可见的颗粒物(被描述为晶状颗粒、白色漂浮物或沉淀物)。
在目视检查以下批次的对照样本时,观察到晶状颗粒/白色物质漂浮/沉淀物:
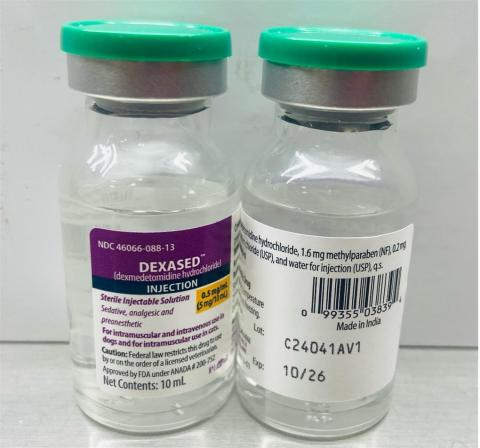
-Dexased™:盐酸右美托咪定注射液 0.5mg/ml(Aspen),NDC 编号:46066-088-13,批次编号:C24041AV1,Mfg。日期:2024 年 11 月,到期日期:2026 年 10 月。
-发行日期:2024 年 12 月至 2025 年 4 月 4 日
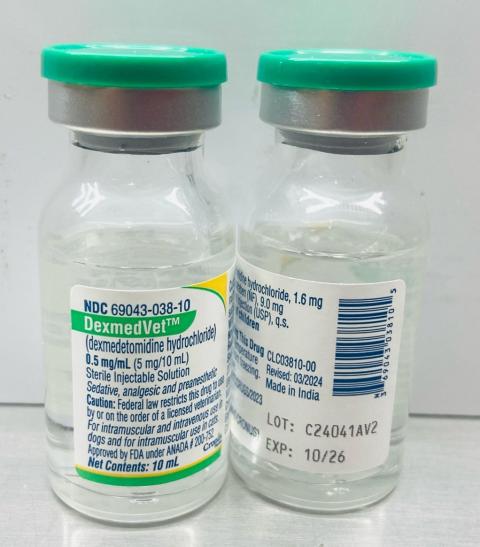
-dexmedVet™:盐酸右美托咪定注射液 0.5mg/ml(Cronus Pharma LLC),NDC 编号:69043-038-10,批次号:C24041AV2,Mfg。日期:2024 年 11 月,到期日期:2026 年 10 月。
-分发日期:2025 年 3 月至 2025 年 4 月 4 日
批号 (LOT) 和到期日期 (EXP) 位于瓶子标签的右下方。
注射含有颗粒物的注射产品可能会导致严重的不良事件。潜在的并发症包括炎症、肉芽肿、纤维化以及心脏、肺部或大脑血管阻塞,这可能导致中风或危及生命的血块事件,包括死亡。总体风险取决于注射途径、颗粒物成分和患者合并症等因素。
不良事件的一些可能体征和症状包括疼痛、虚弱、肿胀、麻痹、发烧、 呼吸困难或呼吸急促、呕吐、活动水平降低、发声或失去知觉。如果您在可能服用本产品的动物身上发现任何这些或任何其他相关症状,请尽快联系兽医。
盐酸右美托咪定注射液0.5 mg/mL被指示用作狗和猫的镇静剂和镇痛剂。
从召回的批次(C24041AV1 和 C24041AV2)中收到 Dexased™(Aspen)和 dexMedVet™(Cronus Pharma LLC)的客户应停止使用这些产品,并参阅您的召回信了解产品退货说明。Cronus Pharma LLC正在与其分销合作伙伴合作,确保未使用的产品不再分销或分销给客户。我们正在直接通知我们的分销商和客户,并正在安排召回的产品的退货。
如果您的动物受到该产品的伤害,请务必举报。它可以帮助检测和解决问题,防止他人受到伤害,还可以进行更好的监控。
来源:www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/cronus-pharma-llc-initiating-voluntary-recall-dexasedtm-aspen-and-dexmedvettm-cronus-pharma-llc
评论
评论