Recall notice
Rappel du Dexased™ et du chlorhydrate de chlorhydrate de Dexmedvet™ pour injection en raison de la présence de particules, USA
il y a 11 mois •source fda.gov
United States
CRONUS PHARMA LLC, au nom de Cronus Pharma Specialties, Hyderabad, Inde, publie un rappel volontaire portant sur un lot comprenant deux lots distincts : Dexased™ (Aspen) et Dexmedvet™ (Cronus Pharma LLC). Les deux produits contiennent du chlorhydrate de dexmédétomidine injectable à 0,5 mg/ml, un produit sur ordonnance aux États-Unis utilisé comme sédatif et analgésique chez les chiens et les chats pour faciliter les examens cliniques, les procédures cliniques, les interventions chirurgicales mineures et les interventions dentaires mineures. Ce produit est également indiqué comme préanesthésique à l'anesthésie générale chez les chiens et les chats.Le rappel est effectué par mesure de précaution en raison de la présence de particules visibles (décrites comme des particules cristallines, de la matière blanche flottante ou des précipités) observées dans la solution.
Des particules ressemblant à des cristaux, des substances blanches flottantes et des précipités ont été observés lors de l'inspection visuelle des échantillons témoins pour les lots suivants :
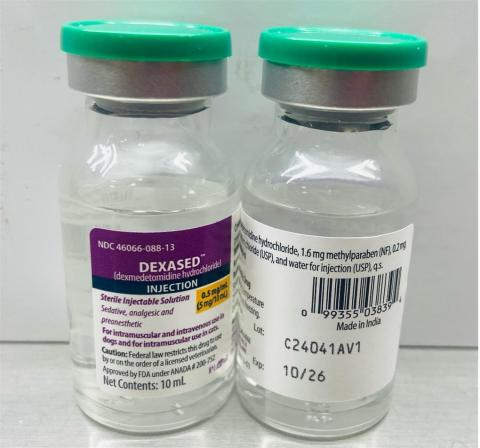
- Dexased™ : chlorhydrate de dexmédétomidine injectable à 0,5 mg/ml (Aspen), numéro NDC : 46066-088-13, numéro de lot : C24041AV1, Mfg. Date : novembre 2024, Exp. Date : octobre 2026.
- Dates de distribution : décembre 2024 au 4 avril 2025
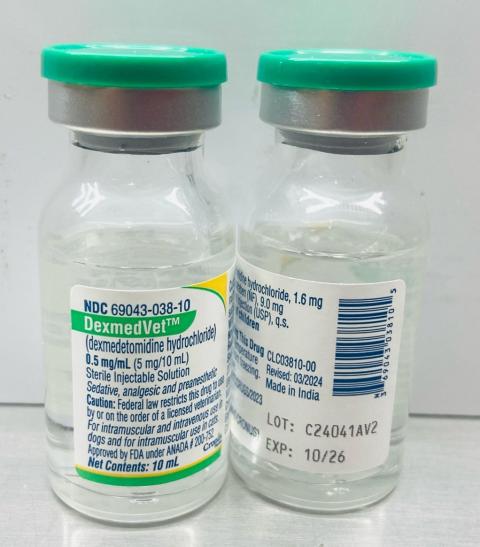
- DexMedVet™ : chlorhydrate de dexmédétomidine injectable à 0,5 mg/ml (Cronus Pharma LLC), numéro NDC : 69043-038-10, numéro de lot : C24041AV2, Mfg. Date : novembre 2024, Exp. Date : octobre 2026.
- Dates de distribution : mars 2025 au 4 avril 2025
Le numéro de lot (LOT) et la date de péremption (EXP) se trouvent dans la partie inférieure droite de l'étiquette du flacon.
L'administration d'un produit injectable contenant des particules peut entraîner des effets indésirables graves. Les complications potentielles incluent l'inflammation, le granulome, la fibrose et l'obstruction des vaisseaux sanguins du cœur, des poumons ou du cerveau, qui peuvent provoquer un accident vasculaire cérébral ou des caillots sanguins potentiellement mortels, voire la mort. Le risque global dépend de facteurs tels que la voie d'injection, la composition des particules et les comorbidités du patient.
Parmi les signes et symptômes possibles d'un événement indésirable, on peut citer la douleur, la faiblesse, l'enflure, la paralysie, la fièvre, respiration difficile ou rapide, vomissements, diminution du niveau d'activité, vocalisation ou perte de conscience. Si vous observez l'un de ces signes ou tout autre signe préoccupant chez un animal auquel ce produit a pu être administré, veuillez contacter un vétérinaire dès que possible.
Le chlorhydrate de dexmédétomidine injectable à 0,5 mg/ml est indiqué pour une utilisation comme sédatif et analgésique chez les chiens et les chats.
Les clients qui ont reçu du Dexased™ (Aspen) et du DexMedVet™ (Cronus Pharma LLC) provenant des lots (C24041AV1 et C24041AV2) faisant l'objet du rappel doivent cesser d'utiliser les produits et consulter votre lettre de rappel pour les instructions relatives au retour des produits. Cronus Pharma LLC travaille avec ses partenaires distributeurs pour s'assurer que les produits non utilisés ne sont plus en distribution ou chez les clients. Nous informons directement nos distributeurs et nos clients et organisons le retour du produit rappelé.
Si ce produit cause des dommages à votre animal, il est important de le signaler. Il peut aider à détecter et à résoudre les problèmes et à empêcher que d'autres personnes ne soient blessées, et il permet une meilleure surveillance.
Une source : www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/cronus-pharma-llc-initiating-voluntary-recall-dexasedtm-aspen-and-dexmedvettm-cronus-pharma-llc
Commentaires
Commentaire