Recall notice
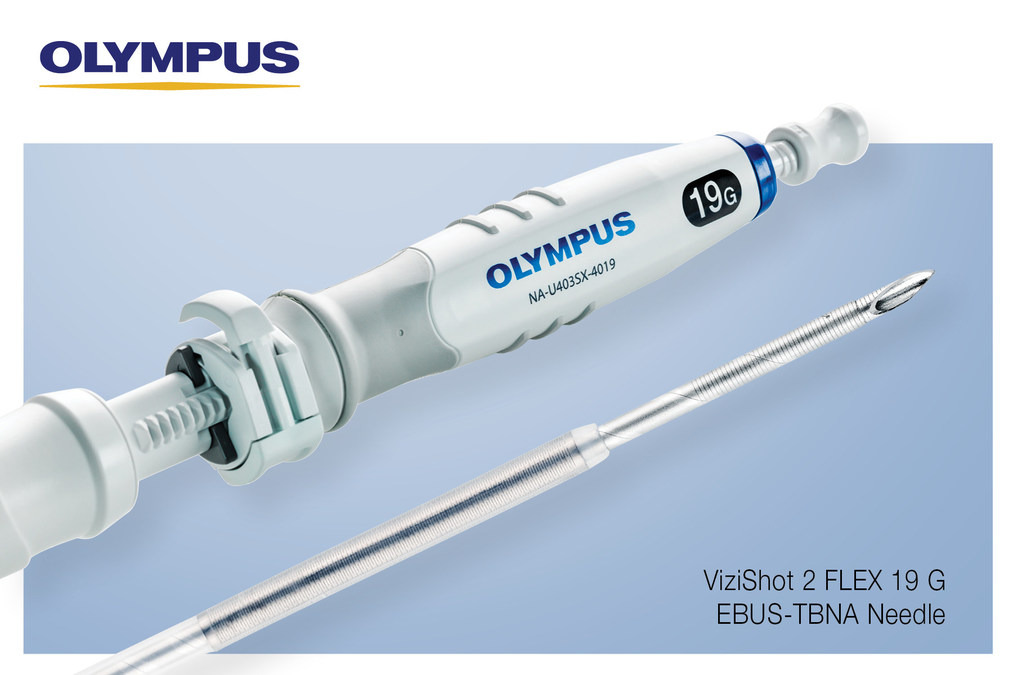
Rappel des aiguilles ViziShot 2 FLEX (19G) EBUS-TBNA en raison de la possibilité que des composants de l'appareil se détachent pendant les procédures, USA
il y a 6 mois •source fda.gov
United States
Mise à jour du 16 janvier 2026 :Olympus a étendu son retrait volontaire mondial des aiguilles EBUS-TBNA ViziShot 2 FLEX (19G) à tous les lots, remplaçant ainsi l'action antérieure d'août 2025 qui ne s'appliquait qu'à des lots spécifiques. Cette extension fait suite à une enquête plus approfondie sur des plaintes concernant des composants de l'appareil éjectés ou se détachant pendant les interventions, y compris des rapports faisant état de blessures chez des patients et d'un décès.
Olympus a identifié d'autres facteurs contributifs affectant tous les lots, notamment la dégradation du matériau thermorétractable et les problèmes liés à l'utilisation, qui peuvent entraîner la rupture des composants, des fuites de liquide, une altération du déploiement ou de la rétraction de l'aiguille et des difficultés à extraire les échantillons.
Les autres aiguilles EBUS-TBNA ne sont pas affectées par cette action.
Une source : www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/olympus-expands-voluntary-recall-vizishot-2-flex-19g-ebus-tbna-needles
22 septembre 2025 :
Olympus Corporation a annoncé une action volontaire et mondiale de retrait des dispositifs médicaux pour les aiguilles VizisHot 2 FLEX (19G) EBUS -TBNA (« VizisHot 2 FLEX ») fabriquées avant le 12 mai 2025, après avoir reçu des rapports faisant état de composants de l'appareil se détachant pendant les procédures.
Le VizisHot 2 FLEX est protégé par un hypotube et une gaine. L'hypotube protège la gaine du bout de l'aiguille et assure la stabilité pendant le transport et l'insertion. Si la gaine a été endommagée et que le dispositif continue d'être utilisé, l'hypotube risque de s'éjecter du dispositif avec les composants en plastique détachés, qui ne sont pas radio-opaques. Des dommages peuvent également survenir pendant le processus de fabrication. Pour améliorer la détection des dommages aux appareils sur le lieu de fabrication, Olympus a mis en place une procédure d'inspection automatisée lors de l'assemblage, une étape qui était auparavant réalisée par le biais d'une inspection visuelle.
Le VizisHot 2 FLEX est conçu pour être utilisé avec des endoscopes à ultrasons pour l'aspiration à l'aiguille fine (FNA) guidée par échographie et la biopsie à l'aiguille fine (FNB) des lésions sous-muqueuses et extramurales de l'arbre trachéobronchique.
Olympus a évalué le problème après avoir reçu des plaintes concernant des effets indésirables impliquant des blessures chez un patient et un décès. Les conséquences potentielles d'un composant détaché du VizisHot 2 FLEX incluent le risque de présence involontaire de composants dans l'arbre trachéobronchique qui peuvent nécessiter une extraction bronchoscopique ou une ablation chirurgicale.
Une source : www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/olympus-issues-voluntary-recall-specific-lots-vizishot-2-flex-19g-ebus-tbna-needles
Commentaires
Commentaire