Recall notice
EzriCare & Delsam Pharma Larmes Artificielles - rappelées en raison d'une contamination microbienne potentielle, USA
il y a 3 ans •source fda.gov
United States
Global Pharma Healthcare rappelle volontairement tous les lots non expirés de leurs Gouttes Oculaires Lubrifiantes Artificial Tears, distribuées par /EzriCare, LLC- et Delsam Pharma, jusqu'au niveau du consommateur, en raison d'une possible contamination. Les Centers for Disease Control and Prevention (CDC) ont alerté la FDA d'une enquête sur un groupe multi-états d'infections à Pseudomonas aeruginosa résistant aux carbapénèmes (VIM-GES-CRPA) produisant des Metallo-β-lactamase médiées par l'Integron de Vérone (VIM) et des β-Lactamase à Spectre Étendu de Guyane (GES), possiblement associées à l'utilisation des larmes artificielles fabriquées par Global Pharma Healthcare. À ce jour, il y a 55 rapports d'événements indésirables incluant des infections oculaires, une perte permanente de la vision, et un décès avec une infection du flux sanguin. Le produit a été distribué à l'échelle nationale aux États-Unis via Internet.Déclaration de Risque : L'utilisation de larmes artificielles contaminées peut entraîner le risque d'infections oculaires qui pourraient résulter en cécité.
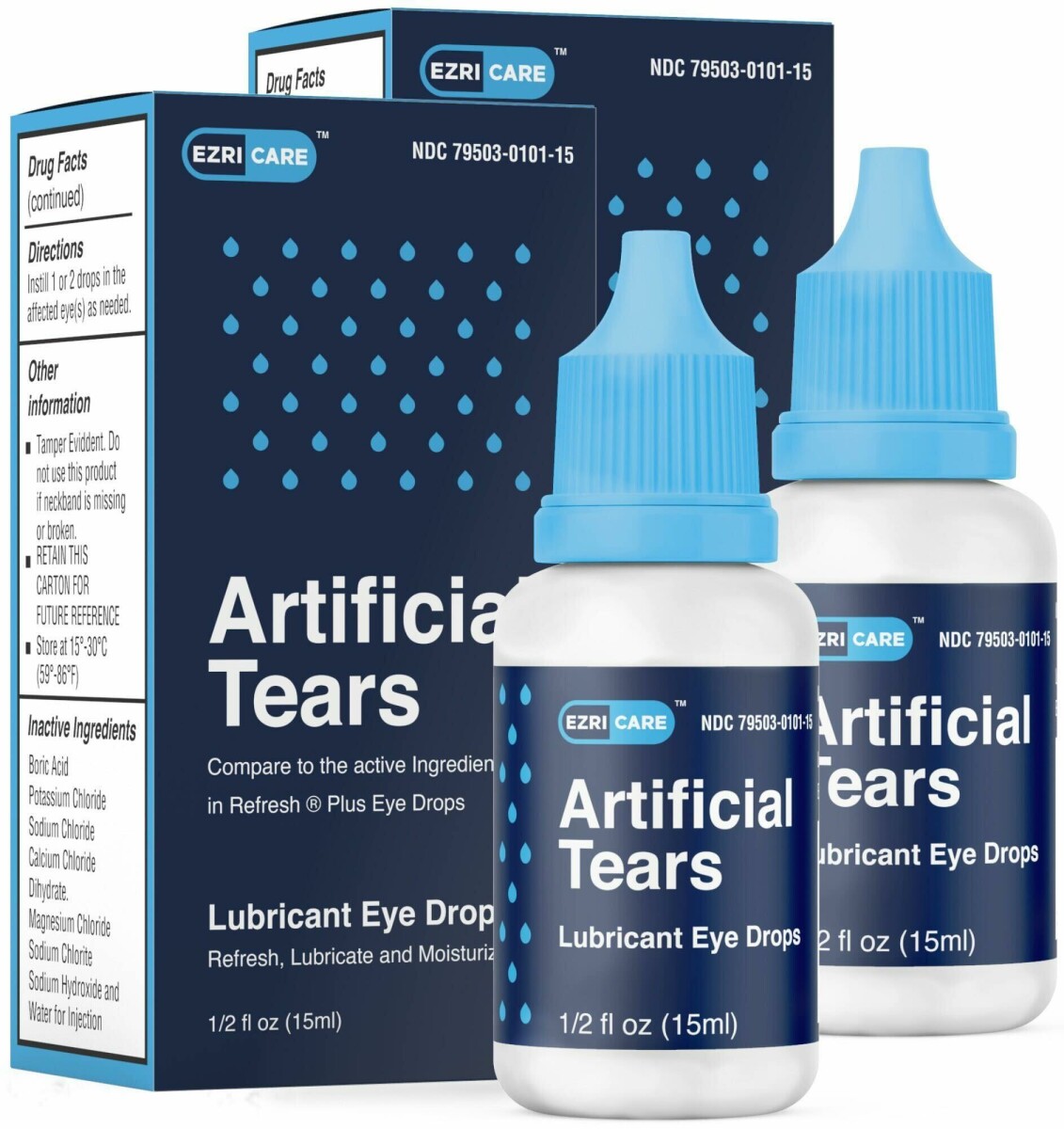
Les Gouttes Oculaires Lubrifiantes Artificial Tears (carboxyméthylcellulose sodique), 10 mg dans 1 mL, flacon de ½ fl oz (15 ml) sont utilisées comme protecteur contre une irritation supplémentaire ou pour soulager la sécheresse de l'œil pour le soulagement temporaire de l'inconfort dû à des irritations mineures de l'œil, ou à l'exposition au vent ou au soleil. Le produit est emballé dans un flacon avec un sceau de sécurité et placé dans une boîte en carton. Il peut être identifié par les photos ci-dessous.
- Ezricare NDC 79503-0101-15. UPC 3 79503 10115 7
- Delsam Pharma's NDC 72570-121-15. UPC -72570-0121-15.
Global Pharma Healthcare notifie les distributeurs de ce produit, Aru Pharma Inc. et Delsam Pharma et demande que les grossistes, détaillants et clients qui ont le produit rappelé cessent son utilisation.
Les consommateurs ayant des questions concernant ce rappel peuvent contacter les distributeurs : Aru Pharma/Ezricare, LLC. Les consommateurs doivent contacter leur médecin ou fournisseur de soins de santé s'ils ont éprouvé des problèmes qui pourraient être liés à l'utilisation de ces produits pharmaceutiques en vente libre.
Nom de l'entreprise : Global Pharma Healthcare
Nom de marque : EzriCare & Delsam Pharma
Produit rappelé : Gouttes Oculaires Lubrifiantes Artificial Tears
Raison du rappel : Contamination microbienne potentielle
Date de rappel FDA : 02 février 2023
Source : www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/global-pharma-healthcare-issues-voluntary-nationwide-recall-artificial-tears-lubricant-eye-drops-due
312
Commentaires
Commentaire