Recall notice
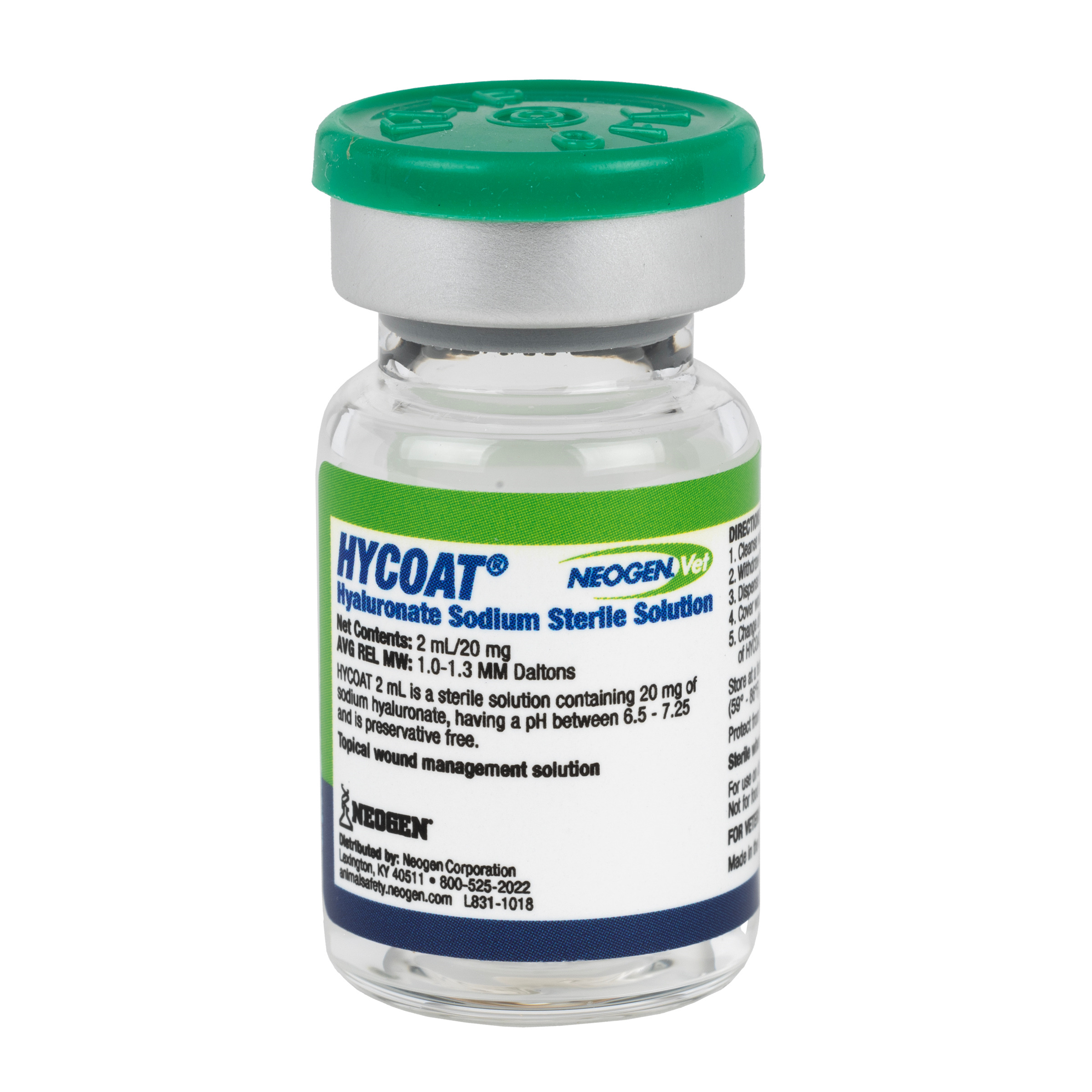
Neogen Vet HYCOAT® Solución Estéril de Hialuronato de Sodio retirada debido a Contaminación Microbiana, USA
hace 2 meses •source fda.gov
United States
Neogen Corporation (NASDAQ: NEOG) está retirando voluntariamente todos los lotes dentro del período de caducidad de la Solución Estéril de Hialuronato de Sodio Neogen®Vet HYCOAT®, para uso en perros, gatos y caballos, a nivel veterinario. Neogen distribuye este producto, que es fabricado por un proveedor tercero. Neogen recibió varios reportes de eventos adversos en caballos después de inyecciones intraarticulares de este producto, lo cual es inconsistente con su uso etiquetado e intencionado. La Solución Estéril de Hialuronato de Sodio Neogen®Vet HYCOAT® fue distribuida a nivel nacional a distribuidores de salud animal y veterinarios.Mientras la investigación de la empresa sobre este problema continúa, por abundante precaución, los viales del producto de 2mL/20mg también están siendo retirados.
Declaración de Riesgo: Este producto está etiquetado como una solución estéril, pero debido a la contaminación microbiana de ciertos lotes, los lotes retirados ya no deben considerarse estériles. Los viales que contienen un contaminante microbiano potencialmente resultan en infección en el animal. El riesgo es particularmente agudo cuando se usa como inyección intraarticular (lo cual es inconsistente con su uso etiquetado e intencionado). También existe riesgo si se usa según la etiqueta como sistema de manejo tópico de heridas en heridas quirúrgicas, quemaduras, úlceras y procedimientos de autoinjerto. Hasta la fecha, Neogen no ha recibido reportes de eventos adversos cuando se usa de manera consistente con el uso etiquetado.
El producto está destinado para uso como sistema de manejo tópico de heridas y está empacado en viales de 2mL/20 mg (Código UPC 726087089386) y 10mL/50mg (Código UPC 726087089393).
Los lotes del producto sujeto dentro del período de caducidad incluyen los siguientes:
Números de lote de 2 mL/20 mg: 0236735, 0236736, 0336746, 0336747, 0536760, 0536761, 0636768, 0636769, 0836792, 0836785, 0836788, 0836789, 0936794, 0936795, 1036801, 1036802, 1036803, 1036804, 1136807, 1136808, 0246837, 0246838, 4L001B, 4L002
Números de lote de 10 mL/50 mg: 0136731, 0736777, 0346843, 5A001
Este retiro ha sido iniciado debido a contaminación microbiana en ciertos lotes de viales del producto de 10 mL/50 mg.
Comentarios
Comentario