Recall notice
Prueba rápida de antígeno del SARS-CoV-2 Flowflex™ (autoprueba): retirada del mercado debido a una distribución no autorizada en EE., USA
hace 4 años •source fda.gov
United States
ACON Laboratories, Inc. («ACON Laboratories»), el fabricante legal de la «Prueba casera de antígeno COVID-19 Flowflex™» (Autorización de uso de emergencia de la FDA EUA210494), ha identificado la distribución en los EE. UU. de productos falsificados no autorizados, adulterados y con marca incorrecta que tienen el nombre comercial «Antígeno SARS-CoV-2 Flowflex» Prueba rápida (autoprueba)». ACON Laboratories no importa la «Prueba rápida de antígeno del SARS-CoV-2 Flowflex (autoprueba)» a los EE. UU., ya que solo está autorizada para su venta en Europa y otros mercados, bajo la marca CE. Este comunicado de prensa sirve como anuncio público de que este producto con la marca CE se retirará del mercado estadounidense.La «prueba rápida de antígeno del SARS-CoV-2 Flowflex (autoprueba)» no se puede importar, distribuir ni utilizar legalmente en el mercado estadounidense, ya que no ha sido aprobada, autorizada o autorizada por la FDA. La «Prueba casera de antígeno COVID-19 Flowflex» no se puede importar, distribuir ni utilizar legalmente en el mercado europeo, ya que no tiene la marca CE. Estos dos productos han sido autorizados por la FDA de los EE. UU. y registrados bajo las autoridades de la marca CE por separado bajo diferentes requisitos de registro de productos y, por lo tanto:
- Este retiro no tendrá ningún impacto en la distribución y el uso del marcado CE «Prueba rápida del antígeno del SARS-CoV-2 Flowflex (autoprueba)» en Europa y otros mercados fuera de los EE. UU.
- Este retiro no tendrá ningún impacto en la distribución y el uso de la «Prueba casera de antígeno COVID-19 Flowflex» autorizada por la FDA en los Estados Unidos.
Declaración de riesgo: Las pruebas de antígeno COVID-19 en el mercado estadounidense que carecen de aprobación, autorización o autorización de la FDA pueden representar un riesgo significativo, ya que pueden llevar a resultados de pruebas inexactos, incluidos resultados de pruebas falsos negativos o falsos positivos. Las pruebas de antígeno COVID-19 en Europa sin la marca CE pueden suponer un riesgo significativo, ya que pueden provocar resultados inexactos, incluidos resultados de pruebas falsos negativos o falsos positivos.
Los resultados falsos negativos de las pruebas de antígenos pueden llevar a un diagnóstico tardío o a un tratamiento del SARS-CoV-2, que puede causar daños a las personas, incluidas enfermedades graves y la muerte. Los resultados negativos falsos también pueden llevar a una mayor propagación del virus SARS-CoV-2, incluso cuando las personas se agrupan en cohortes (es decir, se alojan juntas) en la atención médica, la atención a largo plazo y otros centros en función de los resultados falsos de estas pruebas.
Es posible que no se tomen medidas para limitar la exposición en función de resultados falsos negativos, como aislar a las personas, limitar el contacto con familiares y amigos y limitar la capacidad para trabajar. Los resultados positivos falsos de la prueba de antígenos pueden provocar un retraso tanto en el diagnóstico correcto como en el inicio de un tratamiento adecuado para la causa real de la enfermedad de una persona, que podría ser otra enfermedad potencialmente mortal que no sea COVID-19. Los resultados positivos falsos también podrían conducir a una mayor propagación del virus SARS-CoV-2 cuando las personas presuntamente positivas se agrupan en cohortes (es decir, se alojan juntas).
Hasta la fecha, ACON Laboratories no ha recibido ningún reporte de eventos adversos relacionados con los productos que se abordan en este comunicado de prensa público y está emitiendo este retiro por precaución.
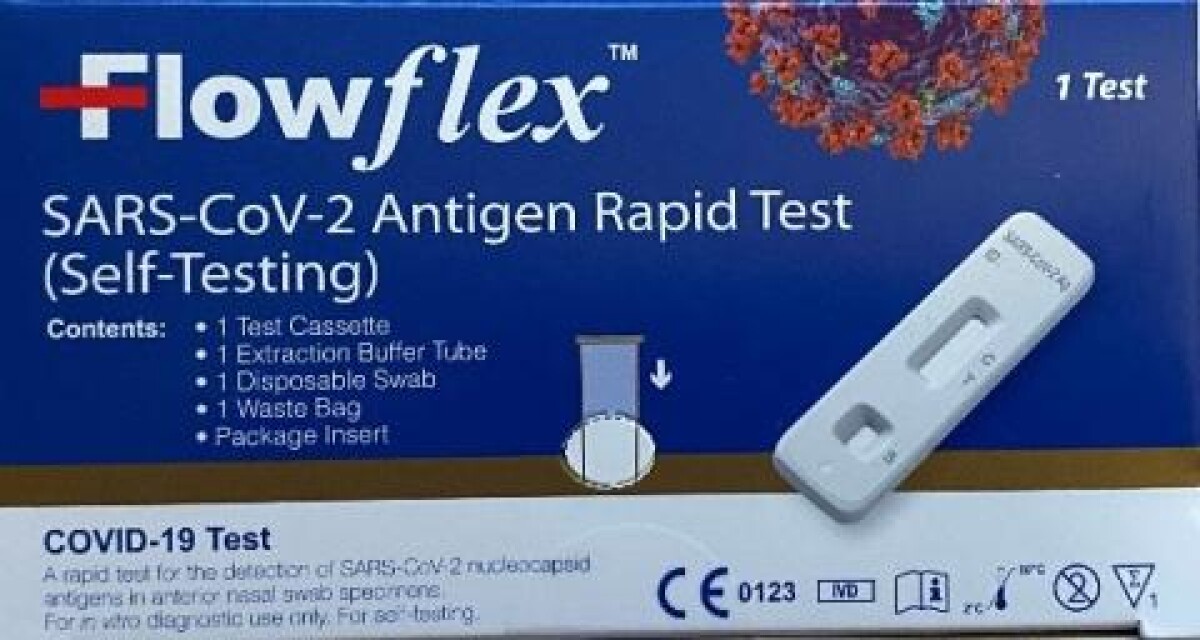
Si ha recibido la «Prueba rápida de antígeno del SARS-CoV-2 Flowflex (autoprueba)» con el recuadro azul en el mercado estadounidense, debe dejar de usar este producto y desecharlo. El producto no ha sido aprobado, autorizado o autorizado para su uso en los EE. UU. Para ayudar a diferenciar el producto retirado del producto autorizado por la FDA, consulte la tabla a continuación, en la que se destacan las diferencias en la etiqueta de la caja del kit del producto. Tenga en cuenta que el producto con la marca CE tiene «ACON Biotech (Hangzhou) Co., Ltd.» como fabricante en lugar de «ACON Laboratories, Inc.»
- Prueba rápida de antígeno del SARS-CoV-2 Flowflex (autoprueba) | No autorizado por la FDA (producto retirado del mercado)
- Prueba casera de antígeno COVID-19 Flowflex | Autorizado por la FDA
Consulte las imágenes de los productos a continuación. ACON trabaja en estrecha colaboración con la FDA y otros organismos encargados de hacer cumplir la ley para garantizar que solo se distribuya en los EE. UU. la «Prueba casera del antígeno COVID-19 Flowflex» autorizada por la FDA. Cualquier distribución de la «Prueba rápida del antígeno del SARS-CoV-2 Flowflex (autoprueba)» debe informarse inmediatamente a ACON Laboratories y a la FDA a los números que se indican a continuación.
Nombre de la compañia: ACON Laboratories, Inc.
Nombre de la marca: Flowflex™
Producto retirado: Prueba rápida de antígeno del SARS-CoV-2 (autoprueba)
Motivo de la retirada: producto falsificado de distribución estadounidense no autorizado
Fecha de retirada de la FDA: 11 de marzo de 2022
Consulta los detalles completos de la retirada en www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/acon-laboratories-issues-recall-non-eua-authorized-flowflextm-sars-cov-2-antigen-rapid-test-self
Fuente: FDA
312
1 Compartir
Comentarios
Comentario