Recall notice
Cápsulas de Etexilato de Dabigatrán de Ascend Laboratories - retiradas debido a la detección de impureza de N-Nitrosodimetilamina, USA
hace 2 años •source fda.gov
United States
Ascend Laboratories LLC. está retirando voluntariamente las Cápsulas de Etexilato de Dabigatrán. USP 75 mg y 150 mg a nivel de consumidor/usuario debido a la presencia de una nitrosamina. N-nitroso-dabigatrán, por encima del nivel establecido de Ingesta Diaria Aceptable (IDA). Los lotes del producto fueron distribuidos a nivel nacional a mayoristas, Distribuidores y Minoristas (dispensadores) en los Estados Unidos desde junio de 2022 hasta octubre de 2022. Hasta la fecha, Ascend Laboratories LLC., no ha recibido ningún informe de eventos adversos relacionados con este retiro.Las nitrosaminas son comunes en el agua y los alimentos, incluyendo carnes curadas y asadas, productos lácteos y vegetales. Todos están expuestos a algún nivel de nitrosaminas. Estas impurezas pueden aumentar el riesgo de cáncer si las personas están expuestas a ellas por encima de niveles aceptables durante largos períodos de tiempo. El producto se usa como anticoagulante oral para reducir el riesgo de accidente cerebrovascular y coágulos sanguíneos.
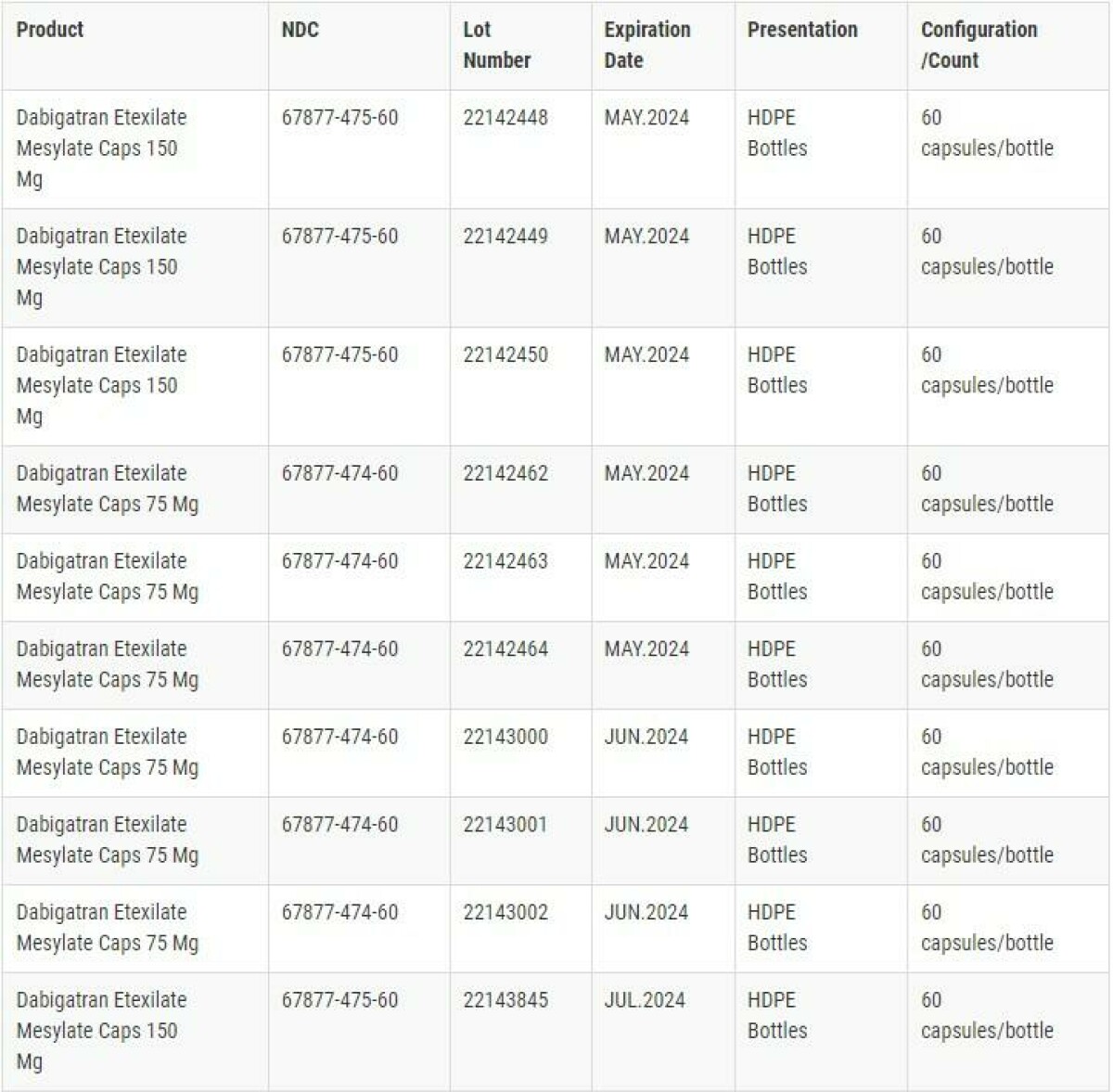
Los detalles de NDC. Número de Lote. Fecha de Vencimiento. y Configuración de Empaque para las Cápsulas de Etexilato de Dabigatrán que están sujetas a este retiro se muestran en la imagen a continuación.
Nombre de la empresa: Ascend Laboratories LLC.
Nombre de la marca: Ascend Laboratories
Producto retirado: Cápsulas de Etexilato de Dabigatrán, USP
Razón del retiro: Detección de impureza de N-Nitrosodimetilamina (NDMA)
Fecha de retiro de la FDA: 22 de marzo de 2023
Fuente: www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/ascend-laboratories-llc-issues-voluntary-nationwide-recall-dabigatran-etexilate-capsules-usp-75-mg
312
Comentarios
Comentario