Recall notice
Gélules d'Étexilate de Dabigatran d'Ascend Laboratories - rappelées en raison de la détection d'impureté de N-Nitrosodiméthylamine, USA
il y a 2 ans •source fda.gov
United States
Ascend Laboratories LLC. rappelle volontairement les Gélules d'Étexilate de Dabigatran. USP 75 mg et 150 mg au niveau consommateur/utilisateur en raison de la présence d'une nitrosamine. N-nitroso-dabigatran, au-dessus du niveau établi d'Apport Journalier Acceptable (AJA). Les lots de produits ont été distribués à l'échelle nationale aux grossistes, Distributeurs et Détaillants (dispensateurs) aux États-Unis de juin 2022 à octobre 2022. À ce jour, Ascend Laboratories LLC., n'a reçu aucun rapport d'événements indésirables liés à ce rappel.Les nitrosamines sont courantes dans l'eau et les aliments, y compris les viandes séchées et grillées, les produits laitiers et les légumes. Tout le monde est exposé à un certain niveau de nitrosamines. Ces impuretés peuvent augmenter le risque de cancer si les personnes y sont exposées au-dessus de niveaux acceptables pendant de longues périodes. Le produit est utilisé comme anticoagulant oral pour réduire le risque d'accident vasculaire cérébral et de caillots sanguins.
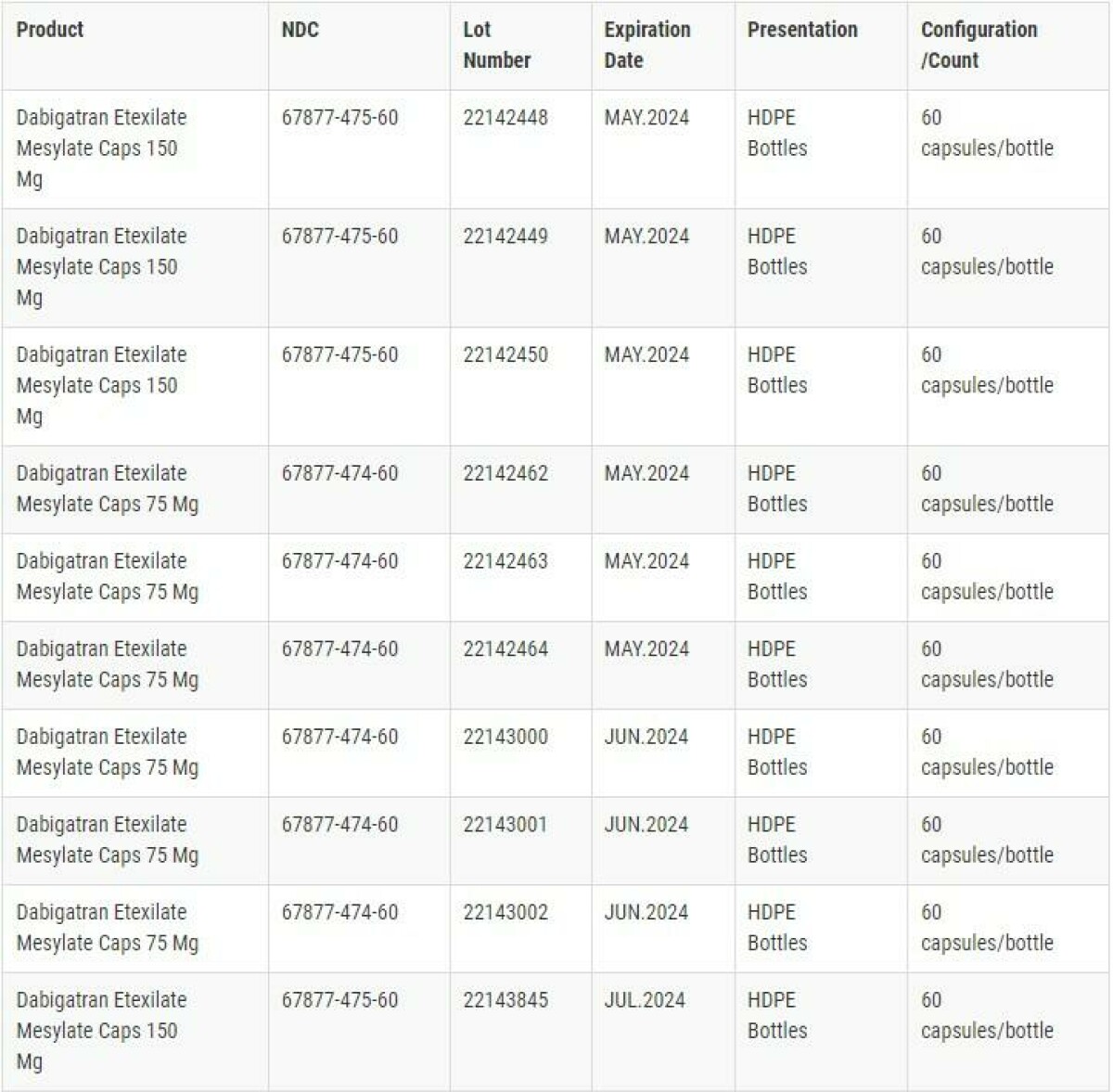
Les détails NDC. Numéro de Lot. Date d'Expiration. et Configuration d'Emballage pour les Gélules d'Étexilate de Dabigatran qui sont soumises à ce rappel sont montrés dans l'image ci-dessous.
Nom de l'entreprise: Ascend Laboratories LLC.
Nom de marque: Ascend Laboratories
Produit rappelé: Gélules d'Étexilate de Dabigatran, USP
Raison du rappel: Détection d'impureté de N-Nitrosodiméthylamine (NDMA)
Date de rappel FDA: 22 mars 2023
Source: www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/ascend-laboratories-llc-issues-voluntary-nationwide-recall-dabigatran-etexilate-capsules-usp-75-mg
312
Commentaires
Commentaire