Recall notice
Nova-Tech Laktat-Ringer-Injektion zurückgerufen aufgrund des Vorhandenseins von faserartigen Partikeln, USA
vor 1 Jahr •source fda.gov
United States
Nova-Tech, Inc. ruft freiwillig eine (1) Charge der Ringer-Laktat-Injektion nur für Tiergebrauch bis zur Endverbraucherebene zurück. Es wurde festgestellt, dass die Ringer-Laktat-Injektion möglicherweise faserartige sichtbare Partikel enthält. Die Ringer-Laktat-Injektion wurde landesweit an Großhändler vertrieben. Das Problem wurde von Nova-Tech während der visuellen Inspektion für Stabilitätstests entdeckt.Risikoerklärung: Die intravenöse Verabreichung eines injizierbaren Produkts, das Partikelmaterial enthält, kann zu schwerwiegenden unerwünschten Ereignissen führen. Mögliche Komplikationen im Zusammenhang mit der Injektion von Partikeln umfassen Venenentzündung, Granulom und Blockierung von Blutgefäßen in Herz, Lunge oder Gehirn, die Schlaganfall oder lebensbedrohliche Blutgerinnsel-Ereignisse einschließlich Tod verursachen können. Die Häufigkeit und Schwere dieser unerwünschten Ereignisse kann je nach verschiedenen Faktoren variieren, einschließlich Größe und Anzahl der Partikel im Arzneimittel, Patientenkomorbiditäten (wie Alter und beeinträchtigte Organfunktion) und Vorhandensein oder Fehlen von Gefäßanomalien.
Einige mögliche Anzeichen und Symptome eines unerwünschten Ereignisses umfassen Schmerzen, Schwäche, Schwellung, Lähmung, Fieber, erschwerte oder schnelle Atmung, Erbrechen, verringerte Aktivität, Lautäußerungen oder Bewusstlosigkeit. Wenn Sie eines dieser oder andere besorgniserregende Anzeichen bei einem Tier beobachten, dem dieses Produkt möglicherweise verabreicht wurde, kontaktieren Sie bitte so schnell wie möglich einen Tierarzt.
BETROFFENES PRODUKT:
- Das Produkt wurde zwischen dem 31. Dezember 2024 und dem 28. Februar 2025 vertrieben.
- Das Produkt wird als injizierbare Lösung nach Anweisung eines Tierarztes verwendet
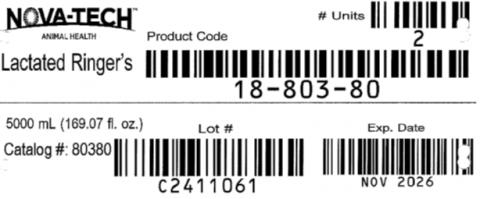
- Ist in 5-Liter-IV-Beuteln mit 2 Einheiten pro Karton verpackt
- Einheiten-UPC 365207803803.
- Die betroffene Ringer-Laktat-Injektion 5-Liter ist Charge # C2411061
- Verfallsdatum NOV 2026.
- Das Produkt kann durch Artikelcode 18-803-80, NDC # 65207-803-80 identifiziert werden.
Verbraucher sollten ihren Tierarzt kontaktieren, wenn sie Probleme erfahren haben, die mit der Einnahme oder Verwendung dieses Arzneimittels zusammenhängen könnten.
Bemerkungen
Kommentar