Regulierungsbericht
Fresenius Kabi USA, LLC Ketorolac Tromethamin Injektion, USP, 30 mg/ml, und Ketorolac Tromethamin Injektion, USP, 60 mg/2 ml - aufgrund von Partikeln zurückgerufen, Fresenius Kabi USA LLC, Corporate Drive, Lake Zurich, IL, USA
vor 6 Jahren •source fda.gov • geschäft
3 Corporate Drive, Lake Zurich, 60047 Illinois, United States
Firmenname: Fresenius Kabi USA, LLCMarkenname: Fresenius Kabi
Zurückgerufene Ware: Ketorolac Tromethamin Injektion, USP, 30 mg/ml, und Ketorolac Tromethamin Injektion, USP, 60 mg/2 mL
Grund für den Rückruf: Vorhandensein von Feinstaub
FDA Rückrufdatum: 20. April 2020
Rückrufdetails: Fresenius Kabi USA, LLC erinnert freiwillig an 13 Lose Ketorolac Tromethamin Injektion, USP, 30 mg/ml, 1 ml füllen in einer 2 ml Bernstein-Durchstechflasche und Ketorolac Tromethamin Injektion, USP, 60 mg/2 ml (30 mg/ml), 2 ml füllen Sie eine 2 ml Bernstein-Durchstechflasche auf Benutzerebene aufgrund der Anwesenheit von Partikeln bestehend aus den folgenden Elementen: Kohlenstoff, Silizium, Sauerstoff und Polyamide.
Feinstaub wurde in acht Reserveprobenfläschchen gefunden. Die Verabreichung von partikelhaltigen Produkten könnte Blutgefäße behindern und zu lokalen Reizungen der Blutgefäße, Schwellungen an der Injektionsstelle, einer Masse von Gewebe, das sich entzünden und infizieren könnte, Blutgerinnsel in die Lunge, Narbenbildung des Lungengewebes und allergische Reaktionen, die zu lebensbedrohlichen Folgen führen könnten.
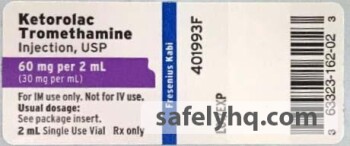
Ketorolac Tromethamin, ein nichtsteroidales entzündungshemmendes Medikament, ist indiziert für die kurzfristige (bis zu 5 Tage bei Erwachsenen) Behandlung von mäßig starken akuten Schmerzen, die eine Analgesie auf Opioid-Ebene erfordert. Die gesamte kombinierte Dauer der Anwendung von Ketorolac Tromethamin und Ketorolac Tromethamin Injektion sollte 5 Tage nicht überschreiten. Im Folgenden finden Sie eine Tabelle der zurückgerufenen Lose, die zwischen dem 5. Mai 2018 und dem 16. Dezember 2019 bundesweit an Großhändler, Distributoren, Krankenhäuser und Apotheken verteilt wurden, sowie eine Kopie des Etiketts:
- Ketorolac Tromethamin Injektion, USP, 30 mg/ml, 1 ml füllen Sie eine 2 ml Amber Durchstechflasche. NDC: 63323-162-01. Produkt-Code: 160201 (Überprüfen Sie die Rückrufbenachrichtigung auf bestimmte Chargennummern)
- Ketorolac Tromethamin Injektion, USP, 60 mg/2 ml (30 mg/ml), 2 ml füllen Sie eine 2 ml bernsteinfarbene Durchstechflasche. NDC: 63323-162-02. Produkt-Code: 160202 (Überprüfen Sie die Rückrufbenachrichtigung auf bestimmte Chargennummern)
Überprüfen Sie die vollständige zurückgerufene Produktliste und Details auf www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/fresenius-kabi-issues-voluntary-nationwide-recall-13-lots-ketorolac-tromethamine-injection-usp-due
Quelle: FDA
1
Bemerkungen
Kommentar