Rapport réglementaire
Fresenius Kabi USA, LLC Ketorolac Trométhamine Injection, USP, 30 mg/mL, et Ketorolac Trométhamine Injection, USP, 60 mg/2 mL - rappelé en raison de la présence de matières particulaires, Fresenius Kabi USA LLC, Corporate Drive, Lake Zurich, IL, USA
il y a 6 ans •source fda.gov • entreprise
3 Corporate Drive, Lake Zurich, 60047 Illinois, United States
Nom de la société : Fresenius Kabi USA, LLCMarque : Fresenius Kabi
Produit rappelé : Ketorolac trométhamine injectable, USP, 30 mg/mL, et Ketorolac trométhamine injectable, USP, 60 mg/2 mL
Motif du rappel : Présence de particules
Date de rappel de la FDA : 20 avril 2020
Détails du rappel : Fresenius Kabi USA, LLC rappelle volontairement 13 lots de Ketorolac Trométhamine Injection, USP, 30 mg/mL, 1 mL remplir un flacon ambre de 2 mL et Ketorolac Tromethamine Injection, USP, 60 mg/2 mL (30 mg/mL), 2 mL remplir un flacon ambre de 2 mL au niveau de l'utilisateur en raison de l'utilisateur en raison de l'utilisateur en raison de la présence de 2 mL composé des éléments suivants : carbone, silicium, oxygène et polyamides.
Des particules ont été trouvées dans huit flacons d'échantillons de réserve. L'administration de produits contenant des particules pourrait obstruer les vaisseaux sanguins et entraîner une irritation locale des vaisseaux sanguins, un gonflement au site d'injection, une masse de tissu qui pourrait devenir enflammée et infectée, des caillots sanguins se rendant au poumon, des cicatrices des tissus pulmonaires et des allergiques qui pourraient entraîner des conséquences potentiellement mortelles.
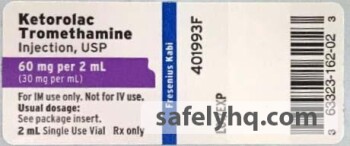
Ketorolac trométhamine, un anti-inflammatoire non stéroïdien, est indiqué pour la prise en charge à court terme (jusqu'à 5 jours chez les adultes) de la douleur aiguë modérément sévère qui nécessite une analgésie au niveau des opioïdes. La durée totale combinée d'utilisation de Ketorolac trométhamine par voie orale et Ketorolac trométhamine par voie orale ne doit pas dépasser 5 jours. Vous trouverez ci-dessous un tableau des lots rappelés distribués à l'échelle nationale aux grossistes, distributeurs, hôpitaux et pharmacies entre le 5 mai 2018 et le 16 décembre 2019, ainsi qu'une copie de l'étiquette :
- Kétorolac Trométhamine Injection, USP, 30 mg/mL, 1 mL remplir dans un flacon ambre de 2 mL. NDC : 63323-162-01. Code produit : 160201. (Vérifiez l'avis de rappel pour les numéros de lot spécifiques)
- Kétorolac Trométhamine Injection, USP, 60 mg/2 ml (30 mg/mL), remplir 2 mL dans un flacon ambre de 2 mL. NDC : 63323-162-02. Code produit : 160202. (Vérifiez l'avis de rappel pour les numéros de lot spécifiques)
Consultez la liste complète des produits rappelés et les détails sur www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/fresenius-kabi-issues-voluntary-nationwide-recall-13-lots-ketorolac-tromethamine-injection-usp-due
Source : FDA
1
Commentaires
Commentaire