监管报告
Fresenius Kabi 美国,有限责任公司酮洛拉克特洛美胺注射液,USP,30 毫克/毫升,和酮罗拉克特洛美胺注射液,USP,60 毫克/2 毫升-由于存在颗粒物质而召回, Fresenius Kabi USA LLC, Corporate Drive, Lake Zurich, IL, USA
6 年前 •source fda.gov • 商业
3 Corporate Drive, Lake Zurich, 60047 Illinois, United States
公司名称:费森纽斯卡比美国有限责任公司品牌名称:费森纽斯卡比
产品回顾:酮罗拉克特洛美胺注射液,USP,30 毫克/毫升,和酮罗拉克特洛美胺注射液,USP,60 毫克/2 毫升
召回原因:存在颗粒物质
林业发展局召回日期:2020 年 4 月 20 日
召回细节:Fresenius Kabi 美国有限责任公司自愿召回 13 批酮洛拉克特洛美胺注射液,USP,30 毫克/毫升,1 毫升填充 2 毫升琥珀瓶和酮洛拉克特洛美胺注射液,USP,60 毫克/2 毫升(30 毫克/毫升),2 毫升填充 2 毫升琥珀瓶,由于颗粒物到用户水平。由以下元素组成:碳、硅、氧和聚酰胺。
在 8 个储备样品瓶中发现颗粒物质。施用含有颗粒物质的产品可能阻碍血管,导致血管局部刺激,注射部位肿胀,组织可能发炎和感染,血块移动到肺部,肺部组织疤痕,过敏可能导致威胁生命的后果的反应。
酮罗拉克曲美胺是一种非甾体抗炎药,用于短期(成人最多 5 天)治疗中度严重急性疼痛,需要在阿片类药物水平镇痛。口服酮罗拉克特洛美胺和酮罗拉克特洛美胺注射剂的总使用持续时间不应超过 5 天。下面列出了 2018 年 5 月 5 日至 2019 年 12 月 16 日期间在全国范围内分发给批发商、分销商、医院和药店的召回批次,以及标签副本:
-酮醇酸甲胺注射液,USP,30 毫克/毫升,1 毫升填充 2 毫升琥珀小瓶。保加利亚国家直接发展委员会的报告:产品代码:160201.(检查召回通知以了解特定批号)
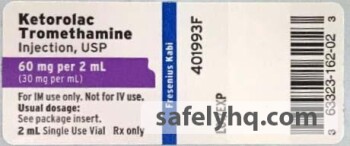
-酮醇酸甲胺注射液,USP,60 毫克/2 毫升(30 毫克/毫升),2 毫升填充 2 毫升琥珀瓶。保加利亚国家直接发展委员会的报告:产品代码:160202.(检查召回通知以了解特定批号)
查看完整的召回产品列表和详细信息,请参阅 www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/fresenius-kabi-issues-voluntary-nationwide-recall-13-lots-ketorolac-tromethamine-injection-usp-due
资料来源:林业发展局
1
评论
评论