Recall notice
سحب حقن هيدروكلوريد الروبيفاكايين بسبب الألياف الخاملة, USA
منذ 11 شهر •source fda.gov
United States
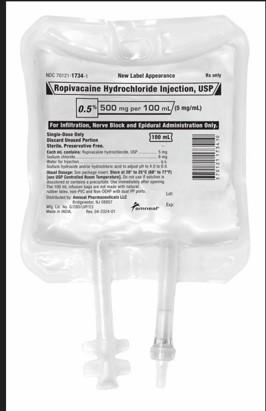
تقوم شركة Amneal Pharmaceutical LLC بسحب دفعتين من حقن هيدروكلوريد الروبيفاكايين، USP، 500 ملغ/100 مل، أكياس التسريب على مستوى المستشفى/المستخدم حيث قد تحتوي المنتجات على ألياف خاملة محددة كألياف البولي بروبيلين من كيس الوريد. تم توزيع المنتج المسحوب على الصعيد الوطني لتجار الجملة/الموزعين فقط بين تواريخ 23/04/2024 إلى 08/11/2024.بيان المخاطر: إدخال جسيمات البولي بروبيلين في الحيز فوق الجافية (أو الإعطاء غير المقصود في الحيز داخل القراب) قد يؤدي إلى مجموعة متنوعة من الأحداث الضارة. هناك احتمال معقول أن المواد الجسيمية في الحيز فوق الجافية قد تسبب عملية التهابية فوق الجافية إلى التهاب السحايا أو قد تضر الحبل الشوكي. عند الإعطاء داخل القراب، قد تؤدي المواد الجسيمية إلى التهاب، استسقاء الرأس (الماء في الدماغ)، مما قد يؤدي إلى الانصمام وتلف الأعضاء.
المنتج مخصص لإنتاج التخدير الموضعي أو الإقليمي للجراحة و/أو إدارة الألم الحاد ومعبأ في أكياس وريدية بجرعة واحدة 12×100 مل (NDC 70121-17343). منتجات حقن هيدروكلوريد الروبيفاكايين المتأثرة، USP، 500 ملغ/100 مل، هي الدفعة AL240003 (انتهاء الصلاحية 01/2026) والدفعة AL240004 (انتهاء الصلاحية 01/2026). لا توجد دفعات أخرى من حقن هيدروكلوريد الروبيفاكايين، USP متأثرة.
تقوم Amneal بإخطار عملائها عبر UPS وتنظم إرجاع جميع المنتجات المسحوبة. يُطلب من تجار الجملة/الموزعين إخطار عملائهم في المستشفيات/المستخدمين بالسحب وتقديم تعليمات للاتصال بـ Amneal لإرجاع المنتجات المسحوبة إلى Amneal.
المصدر: www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/amneal-pharmaceutical-llc-issues-nationwide-recall-ropivacaine-hydrochloride-injection-usp
تعليقات
تعليق