Recall notice
Retiran del mercado las gotas oftálmicas AVKARE por problemas de esterilidad, United States
hace 10 meses •source avkare.com
United States
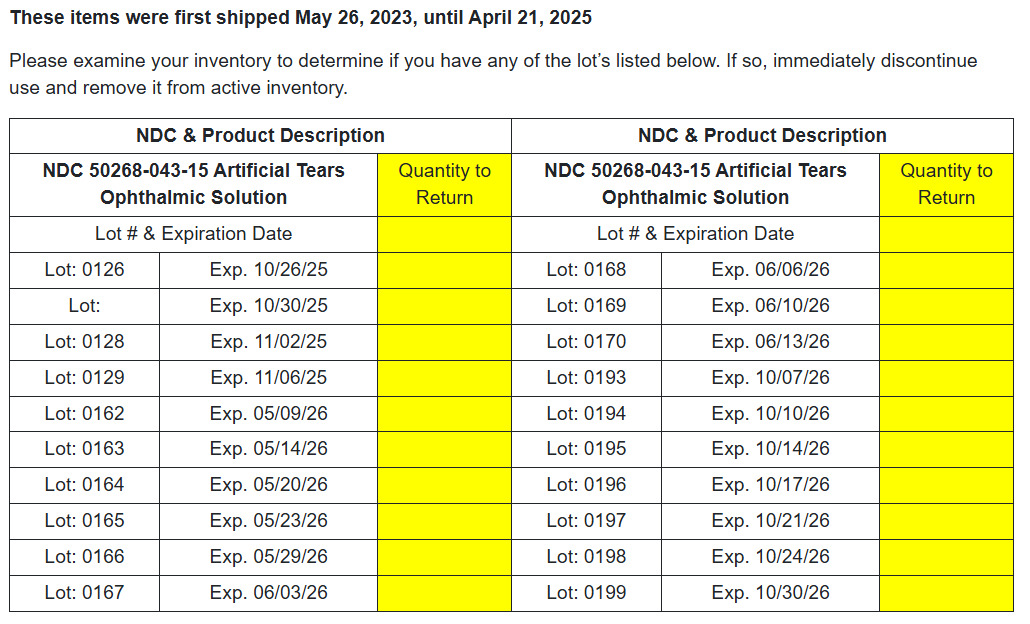
BRS Analytical Service, LLC. ha iniciado un retiro voluntario de varios productos oftálmicos debido a las desviaciones de fabricación identificadas durante una auditoría de la FDA. Actualmente se desconoce el posible peligro para la salud de los usuarios, pero las desviaciones pueden dar lugar a productos de una calidad inaceptable. La retirada se inició después de que la FDA identificara las desviaciones de fabricación durante una auditoría. No se puede descartar el riesgo potencial para los pacientes por el uso de estos productos. La retirada se lleva a cabo con el conocimiento de la Administración de Alimentos y Medicamentos de los Estados Unidos. Los productos se enviaron a nivel nacional entre el 26 de mayo de 2023 y el 21 de abril de 2025. Esto ha cambiado únicamente al nivel minorista.PRODUCTOS AFECTADOS
Solución oftálmica de lágrimas artificiales NDC# 50268-043-15
Gel oftálmico sódico de carboximetilcelulosa NDC# 50268-066-15 1%
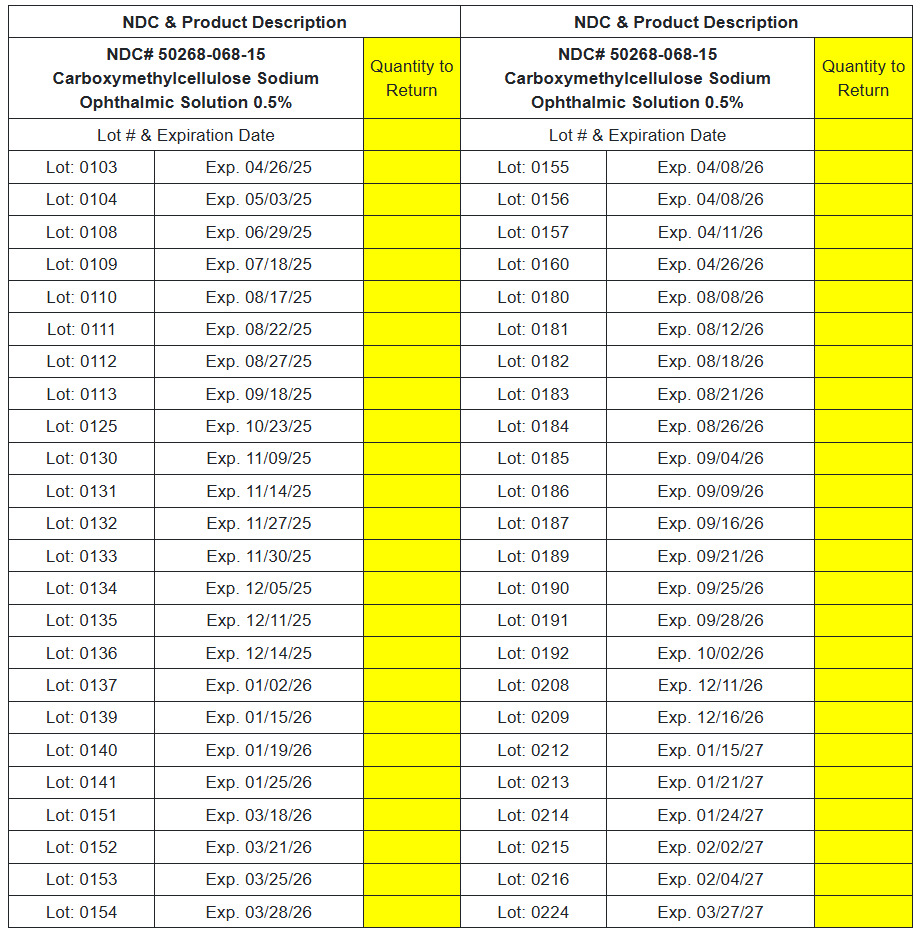
Solución oftálmica sódica de carboximetilcelulosa NDC # 50268-068-15
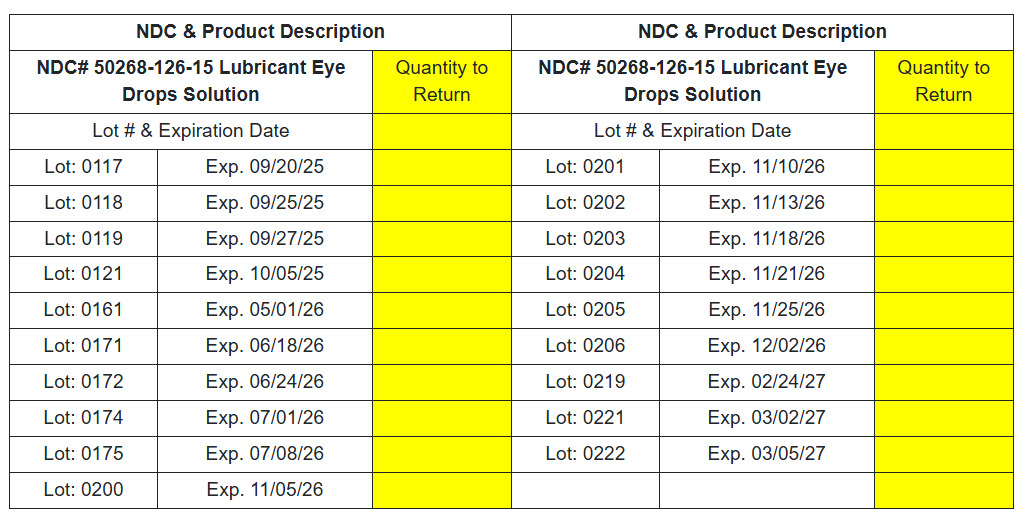
Solución de gotas lubricantes para ojos NDC# 50268-126-15
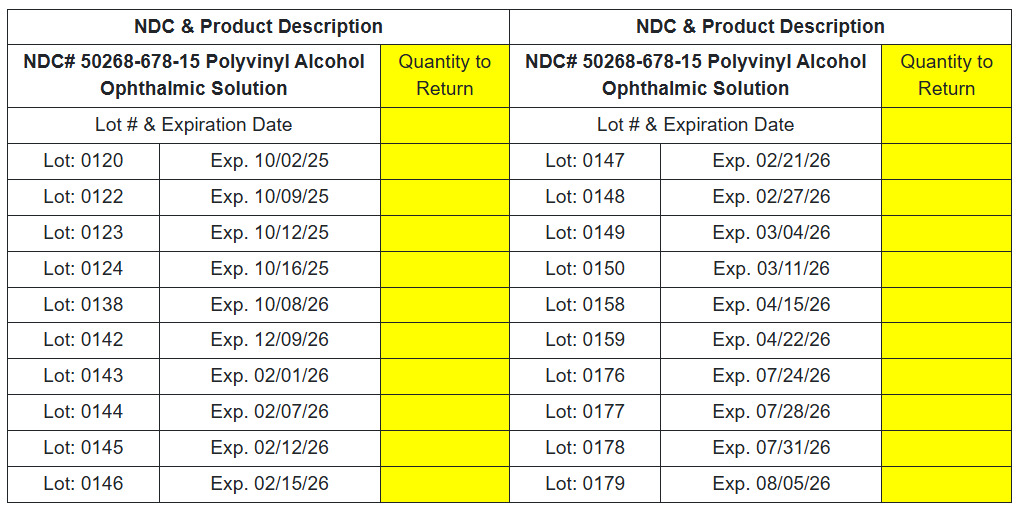
Solución oftálmica de alcohol polivinílico NDC # 50268-678-15
Puedes consultar los detalles del producto afectado en el siguiente enlace.
Se recomienda a los consumidores que no utilicen el producto y que lo devuelvan al lugar donde lo compraron.
Si usted o un ser querido sufre daños o presenta algún síntoma, es importante que lo informe. La presentación de informes puede ayudar a detectar y resolver los brotes de manera temprana y evitar que otras personas sufran daños, y permite una mejor vigilancia. Si los síntomas persisten, busca atención médica.
Fuente: www.avkare.com/recall
22
Comentarios
Comentario