来源:osha.gov | 收据日期:2020-11-19
报告人
Cross Contamination
已更新:
来源:osha.gov | 收据日期:2020-11-19
Fresenius Kabi USA Dexmedetomidine HCL 在 0.9% 氯化钠注射液中-由于与利多卡因交叉污染而召回, USA
3年前 •source www.fda.gov
Recall notice
Brand name: Fresenius Kabi USA
Product recalled: Dexmedetomidine HCL in 0.9% Sodium Chloride Injection
Reason of the recall: Cross Contamination with Lidocaine
FDA Recall date: November 19, 2020
Recall details: Fresenius Kabi USA is voluntarily recalling a single lot of Dexmedetomidine HCl
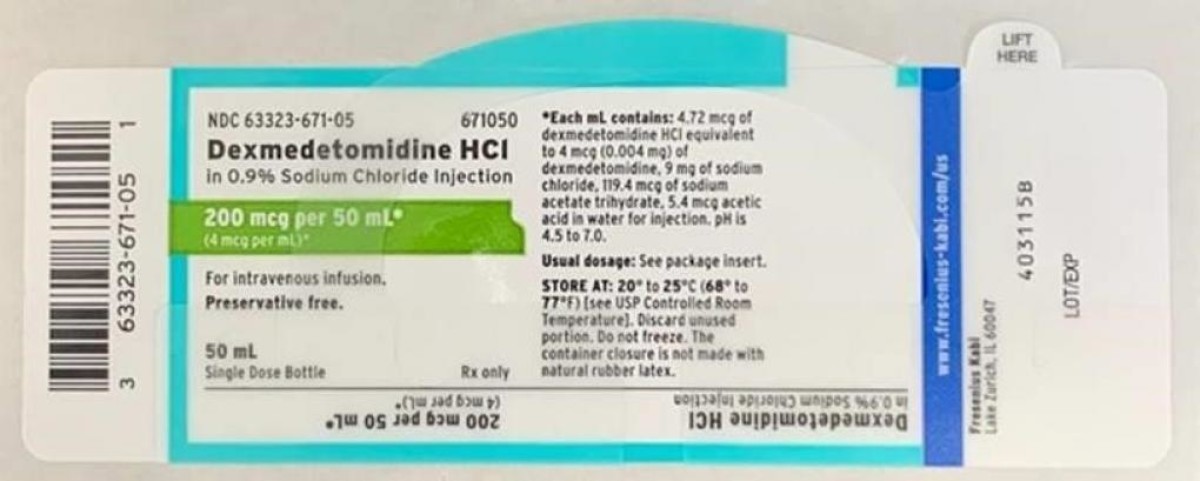
Dexmedetomidine Hydrochloride in 0.9% Sodium Chloride Injection is approved for intravenous use and indicated for sedation of non-intubated patients prior to and/or during surgical and other procedures. Listed below is a table of the recalled lot distributed nationwide to wholesalers, distributors, hospitals and pharmacies between April 9, 2020 and April 13, 2020. An image of the label is also included below.
- Dexmedetomidine HCl in 0.9%. Sodium Chloride Injection, 200 mcg / 50 mL (4 mcg / mL), 50 mL fill in a 50 mL vial. NDC Number: 63323-671-50. Product Code: 671050. Batch number: 6123925. Expiration Date: 03/2022. First Ship Date: 04/09/2020. Last Ship Date: 04/13/2020
Fresenius Kabi is notifying its distributors and customers by letter and asking them to check their stock immediately and to quarantine and discontinue the use and distribution of any affected product.
Distributors should notify their customers and direct them to quarantine and discontinue distributing or dispensing any affected lots, and to return the product to Fresenius Kabi.
Customers with questions regarding this recall may contact Fresenius Kabi at 1-866-716-2459 Monday through Friday, during the hours of 8:00 a.m. to 5:00 p.m. Central Time. Consumers should contact their physician or health care provider if they have experienced any problems that may be related to taking or using this drug product.
Check the full recall details on www.fda.gov
Source: FDA
最近有趣的报告
我订购了一副可拨号眼镜,但它们是垃圾眼镜!!我想退款!, Roy, UT, USA
1周前 •reported by user-dpcr9427
未订购的包裹, Albany, NY, USA
1周前 •reported by user-gwxcb771
召回的商品包含以下信息。产品代码和有效期可以在包装底部找到。
产品名称:Eva Nutrition MexicanteJocote 根,序列号:181121U,制造日期:2023 年 1 月 8 日,有效期:2025 年 6 月 6 日
产品名称:墨西哥 Alpha Tejocote 根的科学,序列号:181121U,制造日期:2023 年 1 月 8 日,到期日期:2025 年 6 月 6 日
产品名称:NWL Nutra 墨西哥 Tejocote 根,序列号:181121U,制造日期:2023 年 1 月 8
产品名称:Niwali 墨西哥 Tejocote 根,序列号:181121U,制造日期:2023 年 1 月 8 日,到期日期:2025 年 6 月
根据24年3月12日发布的安全警报更新,“FDA继续收到与本安全警报中提及的产品相关的不良事件报告。”
此次召回是该公司例行抽样计划的结果,该计划显示成品中含有黄夹竹桃。该公司已停止生产和分销该产品,因为该公司仍在继续调查问题的原因。此外,该公司正在进行全面的质量控制和监测流程。
购买这些产品的客户应立即停止使用它们,并将它们退回购买点以获得全额退款。
摄入黄夹竹桃会对神经系统、胃肠道和心血管健康造成不良影响,这些影响可能很严重,甚至是致命的。症状可能包括恶心、呕吐、头晕、腹泻、腹痛、心脏变化、心律失常等。
如果您在食用本产品后出现症状,请务必报告。它可以帮助及早发现和解决疫情,防止他人受到伤害,还可以进行更好的监测。如果症状持续存在,请就医。
公司名称:Global Mix, Inc.
品牌名称:Eva Nutrition、Alpha Science、Niwali、NWL Nutra
产品召回:Tejocote 膳食补充剂
召回原因:产品含有有毒的黄夹竹桃。
美国食品药品管理局召回日期:2024 年 4 月 10 日
来源:www.fda.gov
艾米丽·亨特寄来的手链, Seattle, WA, USA
2周前 •reported by user-ymnf1212
无包裹, Durham, North Carolina, USA
2周前 •reported by user-qcchx737
https: //risktic.com
我在网上买了衣服但却随机收到了一枚戒指, Iowa, USA
4周前 •reported by user-znztg217
我报告说我收到了 Agra 莫桑石戒指, Wiggs Road, Riverwood NSW, Australia
4周前 •reported by user-fftvz485
我今天在邮件中收到了一个我从未听说过也没有订购的包裹。, Eastpointe, MI, USA
4周前 •reported by user-wjzp6244