Fuente: Osha.gov | Fecha de Recepción: 2020-11-19
Informe por
Cross Contamination
Actualizado:
Fuente: Osha.gov | Fecha de Recepción: 2020-11-19
Fresenius Kabi USA Dexmedetomidina HCL en 0,9% de Cloruro de Sodio Inyección - recuperado debido a la contaminación cruzada con Lidocaína, USA
hace 3 años •source www.fda.gov
Recall notice
Nombre de la marca: Fresenius Kabi USA
Producto retirado: Dexmedetomidina HCL en inyección de cloruro sódico al 0,9%
Motivo del retiro: Contaminación cruzada con Lidocaína
Fecha de retirada de la FDA: 19 de noviembre de 2020
Recordemos detalles: Fresenius Kabi USA
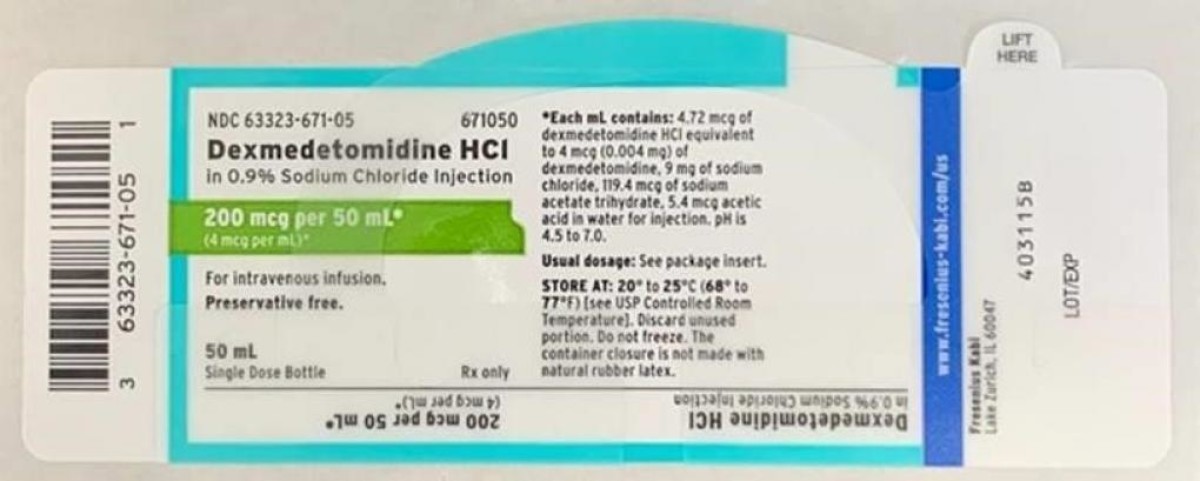
El clorhidrato de dexmedetomidina en inyección de cloruro sódico al 0,9% está aprobado para uso intravenoso e indicado para sedación de pacientes no intubados antes y/o durante procedimientos quirúrgicos y de otro tipo. A continuación se muestra una tabla del lote retirado distribuido a nivel nacional a mayoristas, distribuidores, hospitales y farmacias entre el 9 de abril de 2020 y el 13 de abril de 2020. Una imagen de la etiqueta también se incluye a continuación.
- Dexmedetomidina HCl en 0,9%. Inyección de cloruro de sodio, 200 mcg/ 50 mL (4 mcg/mL), 50 mL llenan un vial de 50 mL. Número NDC: 63323-671-50. Código de Producto: 671050 Número de lote: 6123925. Fecha de caducidad: 03/2022. Fecha del primer envío: 04/09/2020. Fecha del último envío: 04/13/2020
Fresenius Kabi notifica a sus distribuidores y clientes por carta y les pide que comprueben inmediatamente sus existencias y pongan en cuarentena y suspendan el uso y distribución de cualquier producto afectado.
Los distribuidores deben notificar a sus clientes y dirigirlos a poner en cuarentena y suspender la distribución o distribución de los lotes afectados, y devolver el producto a Fresenius Kabi.
Los clientes con preguntas sobre esta retirada pueden ponerse en contacto con Fresenius Kabi al 1-866-716-2459 de lunes a viernes, durante el horario de 8:00 a.m. a 5:00 p.m., hora central. Los consumidores deben ponerse en contacto con su médico o médico si han experimentado algún problema que pueda estar relacionado con tomar o usar este medicamento.
Consulta los detalles completos de la retirada en www.fda.gov
Fuente: FDA
Informes interesantes recientes
Estafado por Heather's Motty, 2207 Summit Avenue, Union City, NJ, USA
hace 3 semanas •reported by user-jxhnt677
Heathers Morty es estafada, por favor no pidas sus productos, Heathers Motty
hace 3 semanas •reported by user-hpypk844
Estafa, Halle (Saale), Germany
hace 3 semanas •reported by user-hkxtw484
No hice el pedido, Texas, USA
hace 3 semanas •reported by user-whyx3942
Recibí el anillo que no pedí, Yoshi deals
hace 2 semanas •reported by user-zjgbv967
No he pedido esto, Montgomery, AL, USA
hace 3 semanas •reported by user-gbmzh111
TECNOLOGÍA 1 - Bright Fire no es eléctrico, 192-01 Northern Blvd, Flushing, NY 11358, U.S.
hace 2 semanas •reported by user-cbjtq248
He recibido un anillo que nunca pedí, Yucca Ave, Lancaster, L A, CA, USA
hace 4 semanas •reported by user-grgz1638
Alerta de estafa, Fontana, CA, USA
hace 3 días •reported by user-jtcfb656