Recall notice
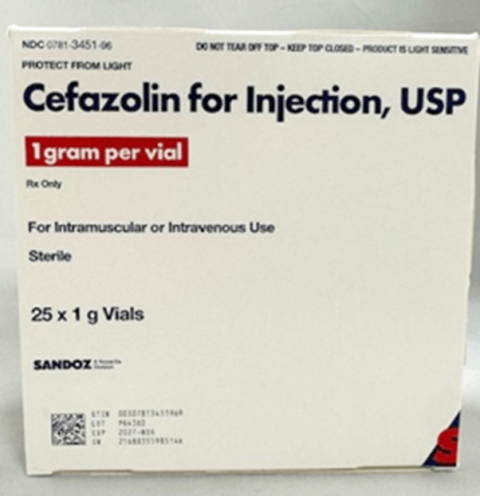
Cefazolina para Inyección, vial de 1 gm retirado debido a Penicilina G Potásica, USA
hace 9 meses •source fda.gov
United States
####Actualización 14 de julio de 2025:Sandoz, Inc. ("Sandoz") está iniciando una expansión de retiro voluntario a nivel nacional de un lote adicional de Cefazolina para Inyección, USP, 1 gramo por vial. El lote está siendo retirado debido a una queja del cliente que indica que cuatro (4) viales etiquetados incorrectamente como Penicilina G Potasio para Inyección, Sandoz ha confirmado que los viales etiquetados incorrectamente como Penicilina G Potasio para Inyección contienen Cefazolina para Inyección, USP, 1 gramo por vial.
Lotes impactados por el retiro voluntario y su expansión:
- Nombre del Producto: Cefazolina para Inyección, USP (25 por viales de 1g)
- NDC del Vial: 0781-3451-70
- NDC del Cartón: 0781-3451-96
- Número de Lote: PG4362
- Fecha de Vencimiento: 2027-NOV
- Fabricante: Sandoz GmbH
- Distribuidor: Sandoz Inc
- Nombre del Producto: Penicilina G Potasio para Inyección, USP
- NDC del Vial: 0781-6136-94
- NDC del Cartón: N/A
- Número de Lote: PG4362
- Fecha de Vencimiento: 2027-NOV
- Fabricante: Sandoz GmbH
- Distribuidor: Sandoz Inc
Fuente: www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/update-sandoz-inc-issues-voluntary-nationwide-recall-expansion-one-additional-lot-cefazolin
27 de junio de 2025:
Sandoz, Inc. ("Sandoz") está iniciando un retiro voluntario de un (1) lote de Cefazolina para Inyección, USP, 1 gramo por vial. Este lote único está siendo retirado debido a una queja del cliente que indica que cuatro (4) viales etiquetados de Penicilina G Potasio para Inyección, USP, 20 millones de Unidades fueron incluidos incorrectamente en un cartón (25 viales por cartón) del producto Cefazolina para Inyección, USP 1 gramo por vial. Sandoz ha recibido una queja de administración inadvertida del producto incorrecto a un paciente.
Declaración de Riesgo: Existe una probabilidad razonable de que la administración inadvertida de inyección de penicilina G potasio, en lugar de la inyección de cefazolina prevista, pueda plantear consecuencias adversas para la salud graves y potencialmente mortales, incluyendo falta de eficacia que lleve a un tratamiento menos que óptimo de infecciones graves, resistencia a antibióticos, reacciones adversas, reacciones alérgicas graves (ej., anafilaxia), interacciones medicamentosas, arritmias cardíacas resultantes del alto potasio especialmente en pacientes con deterioro renal, y recuperación retrasada. El producto que está siendo retirado fue enviado a mayoristas selectos para distribución adicional a nivel nacional.
- Nombre del Producto: Cefazolina para Inyección, USP (25 por viales de 1g)
- NDC del Vial: 0781-3451-70
- NDC del Cartón: 0781-3451-96
- Número de Lote: PG4360
- Fecha de Vencimiento: 2027-NOV
- Fabricante: Sandoz GmbH
- Distribuidor: Sandoz Inc
- Nombre del Producto: Penicilina G Potasio para Inyección, USP
- NDC del Vial: 0781-6136-94
- NDC del Cartón: N/A
- Número de Lote: PG4360
- Fecha de Vencimiento: 2027-NOV
- Fabricante: Sandoz GmbH
- Distribuidor: Sandoz Inc
La Cefazolina para Inyección USP se usa para el tratamiento de infecciones causadas por ciertas bacterias en muchas partes diferentes del cuerpo incluyendo el tratamiento de neumonía. La Cefazolina para Inyección USP también puede usarse para prevenir infecciones, antes y después de cirugía. Los medicamentos antibacterianos como la Cefazolina para Inyección USP tratan solo infecciones bacterianas. No tratan infecciones virales. La Cefazolina para Inyección USP está indicada para pacientes adultos, ancianos, pediátricos, incluyendo recién nacidos a término.
La Penicilina G Potasio para Inyección está indicada en el tratamiento de ciertas infecciones graves incluyendo septicemia, infecciones de piel y heridas. También está aprobada para el tratamiento de difteria, neumonía adquirida en la comunidad, peritonitis, meningitis/abscesos cerebrales, osteomielitis, infecciones del tracto genital, ántrax, tétanos, gangrena gaseosa, listeriosis, pasteurelosis, fiebre por mordedura de rata, fusoespiroquetas, actinomicosis, complicaciones en gonorrea y sífilis y Lyme. Para reducir el desarrollo de bacterias resistentes a medicamentos y mantener la efectividad de la Penicilina G Potasio para Inyección, USP y otros medicamentos antibacterianos, la Penicilina G Potasio para Inyección, USP debe usarse solo para tratar o prevenir infecciones que están probadas o fuertemente sospechadas de ser causadas por bacterias susceptibles. La Penicilina G Potasio para Inyección está indicada para uso en adultos, adolescentes, niños, pediátricos, recién nacidos y prematuros.
Aunque tanto la Cefazolina como la Penicilina G Potasio pertenecen al grupo beta-lactámico de antibióticos, están indicadas para diferentes tipos de infecciones, y el espectro de organismos susceptibles también difiere. Adicionalmente, mientras las poblaciones de pacientes se superponen, cada medicina tiene grupos distintos específicos aprobados, y los regímenes de dosificación pueden diferir también.
Fuente: www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/sandoz-inc-issues-voluntary-nationwide-recall-one-lot-cefazolin-injection-due-product-mispackaging
22
Comentarios
Comentario