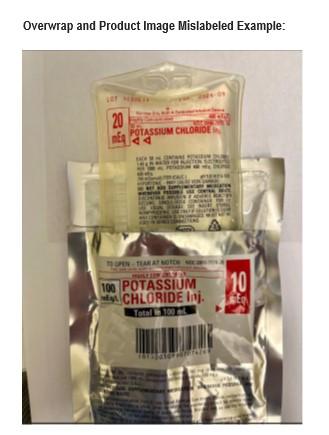
Recall notice
Kaliumchlorid-Injektion zurückgerufen aufgrund von Kaliumchlorid-Überdosierung, USA
vor 5 Monaten •source fda.gov
United States
Otsuka ICU Medical LLC führt einen freiwilligen Rückruf auf Anwenderebene für eine FALSCH ETIKETTIERTE Charge von KALIUMCHLORID Inj. 20 mEq, NDC 0990-7077-14 durch. Das UMHÜLLUNGSETIKETT der Charge 1030613, Verfallsdatum: 30.09.2026 kann das Produkt fälschlicherweise als KALIUMCHLORID Inj. 10 mEq mit NDC 0990-7074-26 identifizieren. Otsuka ICU Medical LLC hat diese Diskrepanz aufgrund eines Herstellungsproblems identifiziert. Die Dosierung ist korrekt auf der Etikettierung gedruckt, die am Produktbeutel angebracht ist, welche nicht sichtbar ist, wenn die 10 mEq UMHÜLLUNG angebracht ist. Diese Benachrichtigung beschreibt das Problem und die erforderlichen Schritte, die Sie durchführen müssen. Die betroffene Produktcharge wurde am 15. April 2025 hergestellt und zwischen dem 23. Mai 2025 und dem 26. August 2025 in den Vereinigten Staaten vertrieben.Wenn die falsche Dosierung auf der 10 mEq Umhüllung anstelle der korrekten 20mEq Dosierung verwendet wird, die auf dem Produkt gedruckt ist, ist eine Überdosierung von Kaliumchlorid möglich. Eine Überdosierung von Kaliumchlorid kann zu Hyperkaliämie führen. Gefahren schwerer Hyperkaliämie nach großen intravenösen Überdosierungen verursachen neuromuskuläre Dysfunktion einschließlich Muskelschwäche, aufsteigende Lähmung, Teilnahmslosigkeit, Schwindel, geistige Verwirrung, Hypotonie, Herzrhythmusstörungen oder Tod durch Herzstillstand. Frühgeborene, Patienten mit chronischer parenteraler Ernährung, Patienten mit einer Vorgeschichte von Herzrhythmusstörungen, Patienten mit chronischer Niereninsuffizienz, Patienten mit akutem Nierenversagen, Patienten mit kaliumsparenden Diuretika—alle sind einem Risiko für unerwünschte und potenziell tödliche Folgen ausgesetzt. Otsuka ICU Medical LLC hat bisher keine Berichte über unerwünschte Ereignisse im Zusammenhang mit diesem Problem erhalten.
Die betroffene Produktcharge (Befindet sich oben links am Produktbeutel oder am Kartonetikett):
- NDC NUMMER: 0990-7077-14
- LISTENNUMMER: 070770452
- PRODUKT: Kaliumchlorid-Injektion 20 mEq
- CHARGENNUMMER: 1030613
- VERFALLSDATUM: 30. September 2026
- KONFIGURATION: 50 mL in flexiblem Behälter
- NDC NUMMER: 0990-7074-26
- LISTENNUMMER: 070740452
- PRODUKT: Kaliumchlorid-Injektion 10 mEq
- CHARGENNUMMER: N/A
- VERFALLSDATUM: N/A
- KONFIGURATION: 100 mL in flexiblem Behälter
BESCHREIBUNG DER ZURÜCKGERUFENEN KARTONS:
- NDC NUMMER: 0990-7077-14
- BARCODE NUMMER: (01)20309907077141
- CHARGENNUMMER: 1030613
- VERFALLSDATUM: 30. September 2026
- KONFIGURATION: 24 pro Karton
Die U.S. Food and Drug Administration (FDA) wurde über diese Maßnahme benachrichtigt.
Quelle: www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/otsuka-icu-medical-llc-issues-voluntary-nationwide-recall-20-meq-potassium-chloride-injection-due
Bemerkungen
Kommentar