Recall notice
Injeção de Cloreto de Potássio recolhida devido a Overdose de Cloreto de Potássio, USA
há 5 meses •source fda.gov
United States
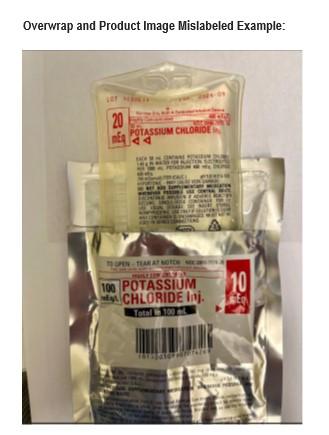
A Otsuka ICU Medical LLC está emitindo um recall voluntário ao nível do usuário, para um lote MAL ROTULADO de CLORETO DE POTÁSSIO Inj. 20 mEq, NDC 0990-7077-14. O rótulo de SOBREMBALAGEM do lote 1030613, Data de Validade: 30-09-2026 pode identificar incorretamente o produto como CLORETO DE POTÁSSIO Inj. 10 mEq com NDC 0990-7074-26. A Otsuka ICU Medical LLC identificou esta discrepância devido a um problema de fabricação. A dosagem está corretamente impressa na rotulagem afixada à bolsa do produto que não é visível quando a SOBREMBALAGEM de 10 mEq está no lugar. Esta notificação detalha o problema e os passos necessários que você deve realizar. O lote de produto afetado foi fabricado em 15 de abril de 2025 e distribuído nos Estados Unidos entre 23 de maio de 2025 e 26 de agosto de 2025.Se a dosagem incorreta na sobrembalagem de 10 mEq for usada em vez da dosagem correta de 20mEq impressa no produto, uma overdose de cloreto de potássio é possível. A overdose de cloreto de potássio pode levar à hipercalemia. Os perigos da hipercalemia severa após grandes overdoses intravenosas causam disfunção neuromuscular incluindo fraqueza muscular, paralisia ascendente, apatia, vertigem, confusão mental, hipotensão, disritmias cardíacas, ou morte por parada cardíaca. Bebês prematuros, pacientes em nutrição parenteral crônica, pacientes que têm histórico de arritmias cardíacas, pacientes com insuficiência renal crônica, pacientes que têm falência renal aguda, pacientes em diuréticos poupadores de potássio—todos estão em risco de resultados adversos e potencialmente fatais. A Otsuka ICU Medical LLC não recebeu relatórios de eventos adversos associados a este problema até o momento.
O lote de produto afetado (Localizado no canto superior esquerdo da bolsa do produto ou no rótulo da caixa é:
- NÚMERO NDC: 0990-7077-14
- NÚMERO DA LISTA: 070770452
- PRODUTO: Injeção de Cloreto de Potássio 20 mEq
- NÚMERO DO LOTE: 1030613
- DATA DE VALIDADE: 30 de setembro de 2026
- CONFIGURAÇÃO: 50 mL em Recipiente Flexível
- NÚMERO NDC: 0990-7074-26
- NÚMERO DA LISTA: 070740452
- PRODUTO: Injeção de Cloreto de Potássio 10 mEq
- NÚMERO DO LOTE: N/A
- DATA DE VALIDADE: N/A
- CONFIGURAÇÃO: 100 mL em Recipiente Flexível
DESCRIÇÃO DAS CAIXAS SENDO RECOLHIDAS:
- NÚMERO NDC: 0990-7077-14
- NÚMERO DO CÓDIGO DE BARRAS: (01)20309907077141
- NÚMERO DO LOTE: 1030613
- DATA DE VALIDADE: 30 de setembro de 2026
- CONFIGURAÇÃO: 24 por caixa
A Food and Drug Administration (FDA) dos EUA foi notificada desta ação.
Fonte: www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/otsuka-icu-medical-llc-issues-voluntary-nationwide-recall-20-meq-potassium-chloride-injection-due
Comentários
Comentário