Ich habe ein Paket erhalten, das nicht bestellt wurde., Florence, SC, USA
vor 4 Wochen •reported by user-ffkt8139
WICHTIG - IHR BERICHT STEHT IN DER WARTESCHLANGE - ES KANN BIS ZU 12 STUNDEN DAUERN, BIS IHR BERICHT AUF UNSERER HOMEPAGE ANGEZEIGT WIRD (WENN ER NICHT ALS PRIVAT BEZEICHNET WURDE).
Besuchen Sie unsere Learn Seiten für weitere hilfreiche Informationen oder senden Sie uns eine E-Mail an: support@safelyhq.com
Mar 12, 2021
Als globale Community-Berichtsplattform, die sich auf das Wohlbefinden der Verbraucher konzentriert, erhalten wir eine Vielzahl von Berichten. Seit der Markteinführung der Covid-19-Impfstoffe haben wir Berichte gesammelt, in denen die Erfahrungen der Menschen nach der Verabreichung von Dosen der derzeit zugelassenen Impfstoffe wie Moderna, Pfizer, Jansen, Johnson & Johnson und Oxford-AstraZeneca wiedergegeben werden. Wir haben uns etwas Zeit genommen, um die bisherigen Ergebnisse zu analysieren und zu kategorisieren, damit wir sie an unsere Community und andere weitergeben können, die dies möglicherweise hilfreich finden
.Wir hoffen, dass sich die Menschen durch die Weitergabe dieser Informationen besser über die Bandbreite der möglichen Folgen ihrer Impfungen informiert fühlen. Für diejenigen, die bereits geimpft wurden, hoffen wir, dass die Ergebnisse einen gewissen Trost bieten, da sie wissen, dass Sie mit bestimmten Nebenwirkungen nicht allein sind.
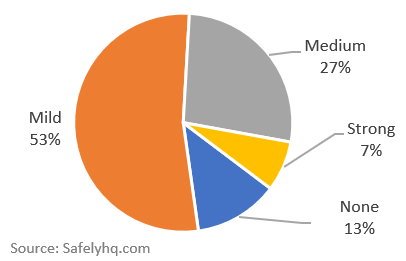
Prozentuale Aufschlüsselung der Covid-19-Nebenwirkungen. Quelle: SafelyHQ.com
Um Berichte zu kategorisieren, haben wir den folgenden Ansatz verwendet:
Wichtig: Der Schwerpunkt dieser Geschichte liegt auf dem Vergleich zwischen Moderna und Pfizer. Bitte beachten Sie unsere Datenhinweise unten zu Meldeverzerrungen und Datenverzerrungen. Wir kommen nicht zu dem Schluss, dass nur 13% der Impfstoffempfänger Nebenwirkungen vermeiden werden.

Vergleich der Covid-19-Nebenwirkungen — Pfizer gegen Moderna. Quelle: SafelyHQ.com
Wir sahen häufiger Berichte ohne Nebenwirkungen von Pfizer, und wo Pfizer-Nebenwirkungen gemeldet wurden, wurden diese häufiger als mild gemeldet als Moderna.
Von Personen, bei denen Nebenwirkungen auftraten, sind die häufigsten Erwähnungen unten aufgeführt. Wir haben Schmerzen ausgeschlossen, da dies in den meisten Berichten üblich war
.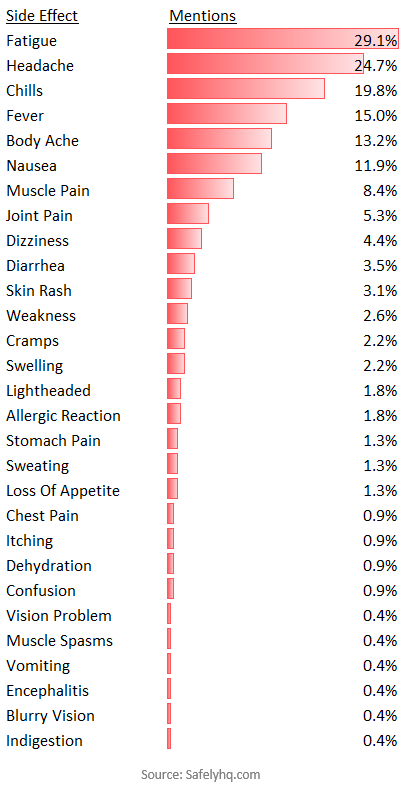
Die am häufigsten gemeldeten Nebenwirkungen des Covid-19-Impfstoffs. Quelle: SafelyHQ.com
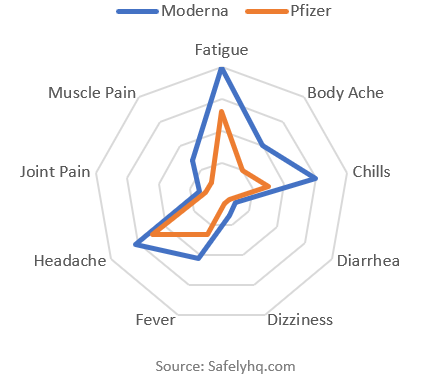
Die 10 häufigsten Erwähnungen zu Nebenwirkungen im Vergleich von Pfizer und Moderna Quelle: SafelyHQ.com
Dies zeigt die zehn häufigsten Erwähnungen nach Impfstoffen (wiederum ohne Schmerzen). Moderna hat mehr Erwähnungen für jede Nebenwirkung. Moderna hat viel mehr Nebenwirkungen pro Bericht erwähnt — insgesamt 60% mehr als Pfizer
.Ein Beispiel für einen Bericht über „Keine Nebenwirkungen“:
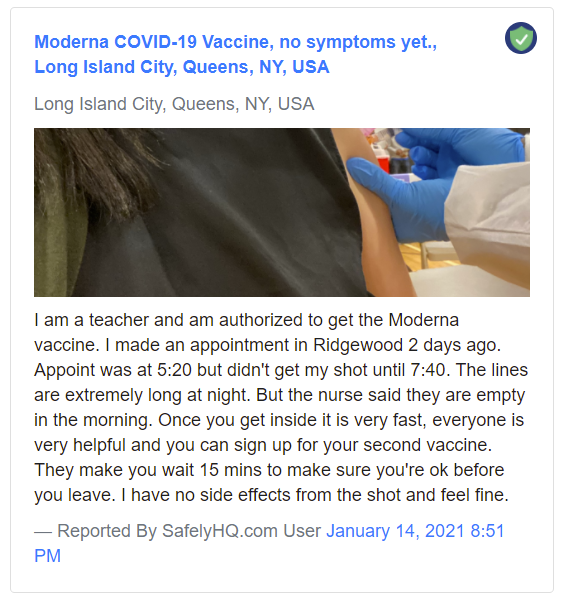
Musterbericht 'Keine Nebenwirkungen'.
Quelle: SafelyHQ.com — LinkEin Beispiel für einen „Mild“ -Bericht:
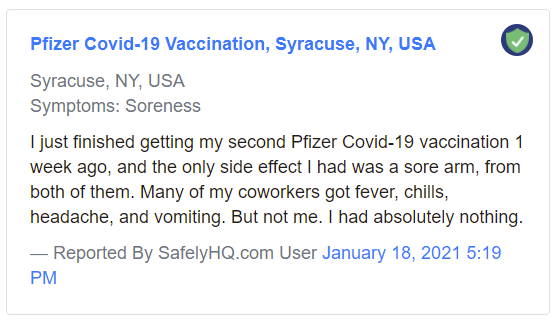
Beispiel für einen „Milden“ -Bericht.
Quelle: SafelyHQ.com — LinkEin Beispiel für einen „Medium“ -Bericht:
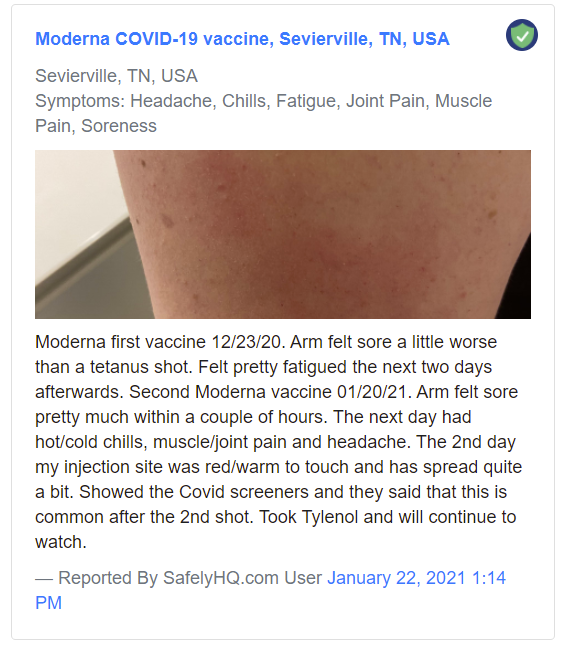
Beispiel für einen 'Medium'-Bericht.
Quelle: SafelyHQ.com — LinkEin Beispiel für einen Bericht über „Starke Nebenwirkungen“:

Beispiel für einen Bericht über „Starke Nebenwirkungen“.
Quelle: SafelyHQ.com — LinkSie können sich gerne in unsere kostenlose E-Mail-Liste eintragen. Erfahren Sie mehr über neue Analysen, erhalten Sie die neuesten Nachrichten und erhalten Sie Updates, sobald neue Berichte eingehen. Um sich anzumelden, klicken Sie hier.
Wir haben Berichte über andere Impfstoffe erhalten, aber bisher liegen nicht genügend Daten vor, um sie in diese Analyse aufzunehmen. Wir würden uns freuen, wenn Sie Ihre Erfahrungen mit uns teilen Sie hatten einen dieser Impfstoffe. Um deine Erfahrung zu teilen, klicke hier.
Sie können die Berichte auf unserer Covid-19-Impfstoff-Landingpage hier einsehen.
Wir laden Sie ein, Ihre Erfahrungen mit uns zu teilen. Gehen Sie einfach auf unsere Landingpage zum Covid-19-Impfstoff und füllen Sie das unten stehende Formular aus. Um zu beginnen, klicken Sie hier
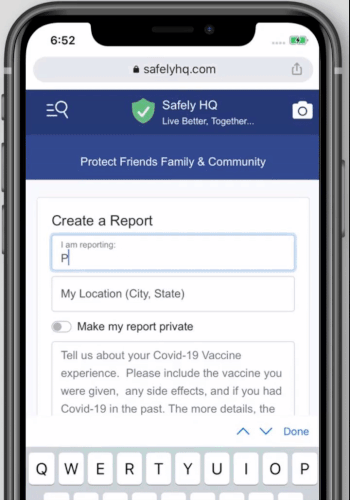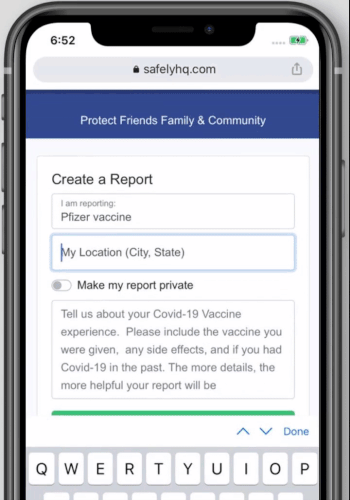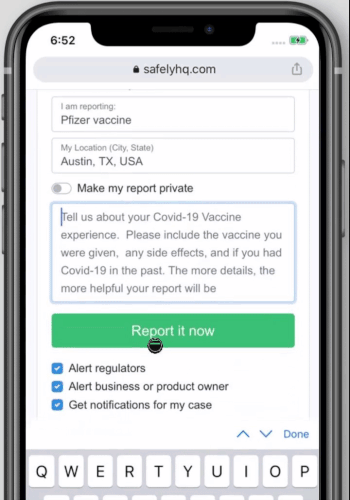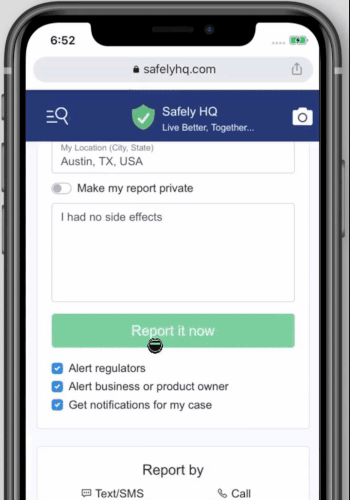
So teilen Sie Ihre Erfahrung mit dem Covid-19-Impfstoff auf safelyhq.com
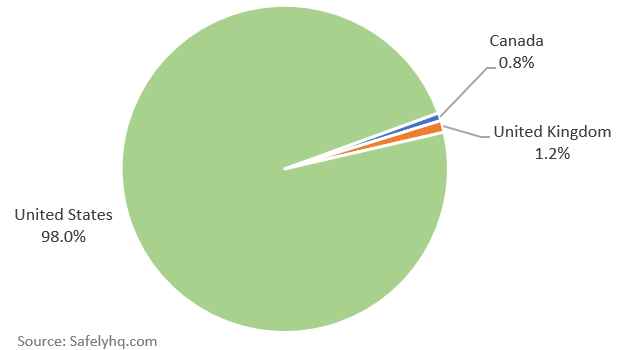
Berichte über Nebenwirkungen des Covid-19-Impfstoffs nach Ländern. Quelle: SafelyHQ.com
Wir haben Berichte aus den meisten Bundesstaaten der USA erhalten, wobei die höchste Beteiligung aus Kalifornien, Texas und Florida kam.
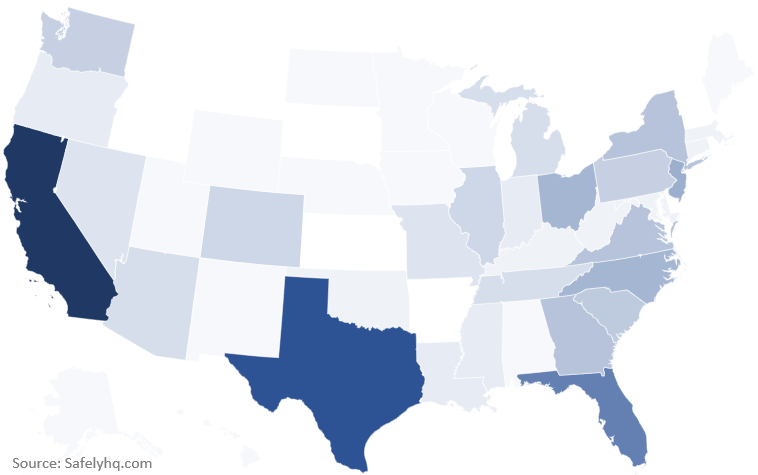
Quelle der US-Covid-19-Impfstoffberichte nach Bundesstaaten. Quelle: SafelyHQ.com
vor 4 Wochen •reported by user-ffkt8139
vor 2 Wochen •reported by user-jttn3275
vor 2 Wochen •reported by user-cbjtq248
vor 2 Wochen •reported by user-ffhdg745
vor 3 Tagen •reported by user-yztyn577
vor 4 Tagen •reported by user-drxjp677
vor 2 Wochen •reported by user-mfmbd859
vor 2 Wochen •reported by user-zcwn4673
vor 3 Tagen •source www.fda.gov
Recall notice
Search