Recall notice
Nostrum Laboratories, Inc. Metformina HCl tabletas de liberación extendida, USP 750 mg - se recuerda debido a los niveles de impurezas de nitrosamina por encima del límite de ADI de 96 ng/día, USA
hace 4 años •source fda.gov
United States
Nombre de la empresa: Nostrum Laboratories, Inc.Nombre de la marca: Nostrum Laboratories, Inc.
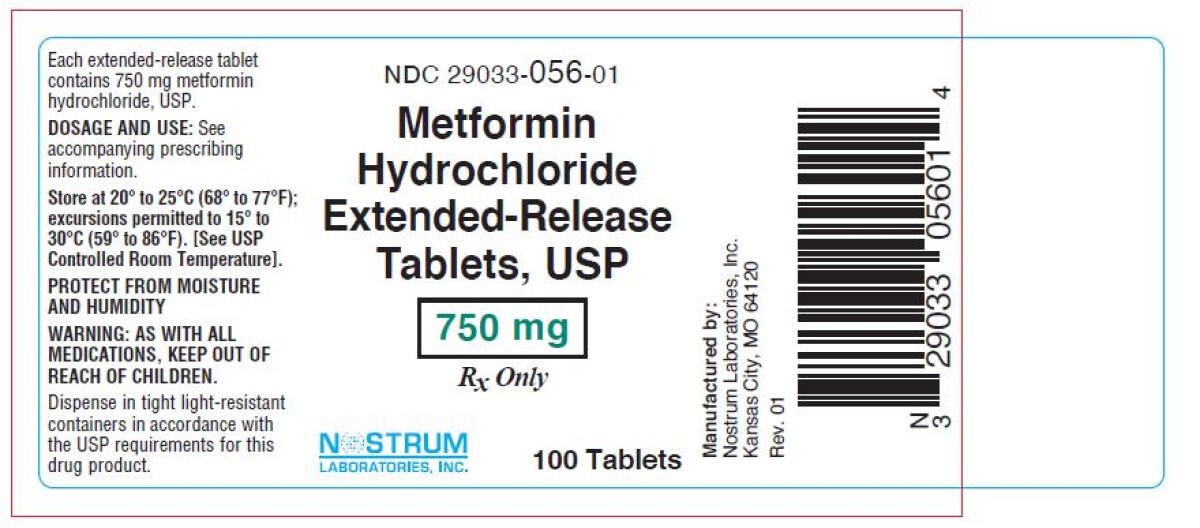
Producto recuperado: Metformina HCl tabletas de liberación extendida, USP 750 mg
Motivo de la retirada: Debido a niveles de impurezas de nitrosamina por encima del límite de IDA de 96 ng/día
Fecha de retirada de la FDA: 25 de enero de 2021
Recordemos detalles: Kansas City, Missouri, Nostrum Laboratories, Inc. está recordando voluntariamente un lote de tabletas de liberación extendida de Metformin HCl, USP 750 mg (equivalente genérico a Glucophage Tablets) al nivel del consumidor. Se ha comprobado que los comprimidos de liberación extendida de Metformina HCl, USP 750 mg (equivalente genérico de Glucophage Tablets) contienen niveles de impurezas de nitrosamina por encima del límite de IDA de 96 ng/día, tal como se publicó en el Documento de Orientación de la FDA publicado en septiembre de 2020. Esta es una ampliación de la retirada anunciada inicialmente el 2 de noviembre de 2020. La NDMA se clasifica como un probable carcinógeno humano (una sustancia que podría causar cáncer) en función de los resultados de pruebas de laboratorio.
El NDMA es un contaminante ambiental conocido y se encuentra en el agua y los alimentos, incluyendo carnes, productos lácteos y verduras. Hasta la fecha, Nostrum Laboratories, Inc. no ha recibido ningún informe de eventos adversos relacionados con este retiro.
El producto está indicado como complemento de la dieta y el ejercicio para mejorar el control de la glucosa en sangre en adultos con diabetes mellitus tipo 2 y se envasa en frascos de HDPE de 100 comprimidos, bajo NDC 29033-056-01. El lote afectado de Metformina HCl Extended Release Tablets, USP 750 mg (equivalente genérico a Glucophage Tablets) se enumera en la siguiente tabla. El producto se puede identificar como un comprimido oblongo blanco roto grabado con «NM7». Metformin HCl Extended Release Tablets, USP 750 mg (equivalente genérico de Glucophage Tablets) se distribuyó a nivel nacional en los Estados Unidos a mayoristas que distribuían más a farmacias y pacientes.
- Descripción del producto: Metformina HCl tabletas de liberación extendida, USP 750 mg (equivalente genérico a tabletas de Glucophage)
- NDC: 29033-056-01
- Número de lote: MET200601
- Fechas de caducidad: 07/2022
Nostrum Laboratories, Inc. notifica a sus distribuidores por carta y está organizando la devolución de todos los productos retirados. Los consumidores con preguntas médicas acerca de esta retirada pueden ponerse en contacto con Nostrum Laboratories, Inc. Medical Affairs en el número de teléfono 816-308-4941 o por correo electrónico quality@nostrumpharma.com de lunes a viernes de 8 am a 5 pm CST. Los consumidores deben ponerse en contacto con su médico o farmacia para obtener más asesoramiento médico.
Consulta los detalles completos de la retirada en www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/nostrum-laboratories-inc-expands-voluntary-nationwide-recall-metformin-hcl-extended-release-tablets-0
Fuente: FDA
312
Comentarios
Comentario