Recall notice
Naturaleza-Throid y WP Tiroid - retirado debido a que el producto puede ser sub potente, United States
hace 5 años •source fda.gov
United States
Nombre de la empresa: RLC Labs, IncNombre de la marca: RLC Labs
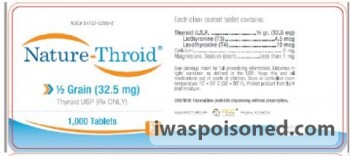
Producto retirado: Nature-Throid® y WP Thyroid®
Motivo de la retirada: el producto puede ser subobpotente
Fecha de retirada de la FDA: 02 de septiembre de 2020
Recuperar detalles: RLC Labs, Inc. está retirando voluntariamente un total de 483 lotes de Nature-Throid® y WP Thyroid® en todas las fortalezas, todos los recuentos de productos dentro de la caducidad actual hasta el nivel de consumo. Los productos están siendo retirados porque las pruebas de muestras de seis (6) lotes realizadas por la Administración de Alimentos y Medicamentos de los Estados Unidos encontraron que las muestras eran subobpotentes. El producto puede tener tan bajo como el 87% de la cantidad etiquetada de Liotironina (T3) o Levotiroxina (T4).
Declaración de Riesgo: Los pacientes tratados por hipotiroidismo (tiroides subactivos), que reciben Nature-Throid® o WP Thyroid®, pueden experimentar signos y síntomas de hipotiroidismo (tiroides subactivos) que pueden incluir fatiga, aumento de la sensibilidad al frío, estreñimiento, piel seca, cara hinchada, pérdida de cabello, ritmo cardíaco lento, depresión, hinchazón de la glándula tiroides y/o aumento de peso inexplicable o dificultad para perder peso. Existe un riesgo razonable de lesiones graves en recién nacidos o mujeres embarazadas con hipotiroidismo, incluyendo aborto espontáneo temprano, hipertiroidismo fetal y/o alteraciones en el desarrollo neural y esquelético fetal. En pacientes de edad avanzada y pacientes con enfermedad cardíaca subyacente pueden ocurrir manifestaciones cardíacas tóxicas de hipertiroidismo, tales como dolor cardíaco, palpitaciones o arritmia cardíaca.
RLC Labs, Inc. no ha recibido ningún informe de eventos adversos relacionados con este retiro. Nature-Throid® y WP Thyroid® (tabletas de tiroides, USP) se compone de liotironina y levotiroxina, y se utilizan para tratar el hipotiroidismo (tiroides subactivos). Los productos sujetos a retirada se envasan en botellas de 30, 60, 90, 100 y 1.000. Para identificar mejor el producto, los NDC, las descripciones del producto, los números de lote y las fechas de caducidad se enumeran en el siguiente enlace.
Estos lotes fueron distribuidos en todo el país en los EE.UU. a las cuentas directas de RLC Labs, Inc. incluyendo profesionales de la salud y farmacias al por menor. RLC Labs, Inc. está notificando proactivamente a sus mayoristas por correo electrónico, correo y teléfono para interrumpir la distribución del producto que se está retirando y está organizando la devolución de todos los productos retirados. Los pacientes que estén tomando Nature-Throid® y WP Thyroid® no deben interrumpir el uso sin ponerse en contacto con su proveedor de atención médica para obtener más orientación y/o prescripción de reemplazo.
Los consumidores que tengan preguntas sobre el retiro pueden enviar un correo electrónico a RLC Labs, Inc. a recall@rlclabs.com o ponerse en contacto con RLC Labs, Inc. Servicio al Cliente al 1-877-797-7997, de lunes a jueves de 7:00am a 4:00pm MST (AZ) y viernes de 7:00am a 3:00pm MST (AZ). Los consumidores deben ponerse en contacto con su médico o proveedor de atención médica si han experimentado algún problema que pueda estar relacionado con tomar o usar este medicamento. Las reacciones adversas o los problemas de calidad experimentados con el uso de este producto pueden ser reportados al programa de informes de eventos adversos MedWatch de la FDA, ya sea en línea, por correo regular o por fax. Complete y envíe el informe en línea.
Correo regular o Fax: Descargue el formulario o llame al 1- 800-332-1088 para solicitar un formulario de notificación, luego complete y regrese a la dirección en el formulario previamente dirigido, o envíelo por fax al 1-800-FDA-0178.
Este retiro se lleva a cabo con el conocimiento de la Administración de Alimentos y Medicamentos de los Estados Unidos.
Consulta los detalles completos de la retirada en www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/rlc-labs-inc-issues-voluntary-nationwide-recall-all-lots-nature-throidr-and-wp-thyroidr-current
Fuente: FDA
312
Comentarios
Comentario