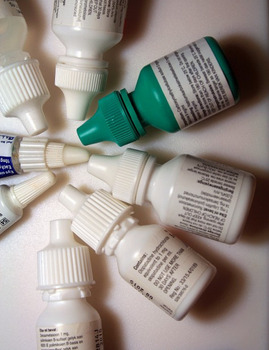
Recall notice
Eye Drop Products recalled due to Lack of Assurance of Sterility, United States
há 2 semanas •source accessdata.fda.gov
United States
K.C. Pharmaceuticals, Inc. has initiated a voluntary recall of various sterile eye drop products due to a lack of assurance of sterility. The products were distributed nationwide in the United States. The recall affects multiple brands and formulations, including those sold under Walgreens, CVS Health, and Good Sense labels. In total, over 2 million bottles are affected by this recall.AFFECTED PRODUCTS:
PRODUCT: Sterile Eye Drops AC
- Size: 0.5 fl oz (15 mL)
- Lot Code: AC24E01
- Expiration Date: 05/31/2026
- Product Quantity: 182,424 bottles
- Multiple brands (e.g., Best Choice, Walgreens, CareOne, TopCare, H-E-B, etc.)
- Contains tetrahydrozoline HCl and zinc sulfate
PRODUCT: Eye Drops Advanced Relief
- Size: 0.5 fl oz (15 mL)
- Lot Codes & Expiration Dates:
AR24D01 – 04/30/2026
AR24G01 / AR24G02 – 07/31/2026
AR24M01 – 10/31/2026
- Product Quantity: 303,216 bottles
- Multiple brands (e.g., Walgreens, Kroger, CVS, TopCare, etc.)
- Contains dextran 70, polyethylene glycol, tetrahydrozoline
PRODUCT: Dry Eye Relief Eye Drops
- Size: 0.5 fl oz (15 mL)
- Lot Codes & Expiration Dates:
LT24E01 / LT24E02 / LT24E03 – 05/31/2026
LT24F01 – 06/30/2026
LT24G01 – 07/31/2026
LT24M01 / LT24M02 – 10/31/2026
- Product Quantity: 1,023,096 bottles
- Multiple brands (e.g., Rite Aid, TopCare, H-E-B, Meijer, etc.)
- Lubricating formula
PRODUCT: Ultra Lubricating Eye Drops
- Size: 0.5 fl oz (15 mL)
- Lot Codes & Expiration Dates:
SU24E01 / SU24E02 / SU24E03 – 05/31/2026
SU24K01 – 09/30/2026
- Product Quantity: 245,184 bottles
- Multiple brands (e.g., Walgreens, CVS, Publix, Kroger, etc.)
- Contains polyethylene glycol and propylene glycol
PRODUCT: Sterile Eye Drops Original Formula
- Size: 0.5 fl oz (15 mL)
- Lot Codes & Expiration Dates:
RG24E01 – 05/31/2026
RG24G01 / RG24G02 – 07/31/2026
- Product Quantity: 378,144 bottles
- Multiple brands (e.g., Walgreens, Kroger, H-E-B, TopCare, etc.)
- Tetrahydrozoline-based formula
PRODUCT: Sterile Eye Drops Redness Lubricant
- Size: 0.5 fl oz (15 mL)
- Lot Codes & Expiration Dates:
RL24D01 – 04/30/2026
RL24F01 / RL24F02 – 06/30/2026
- Product Quantity: 315,144 bottles
- Multiple brands (e.g., Walgreens, Rite Aid, Leader, etc.)
- Redness relief formula
PRODUCT: Sterile Eye Drops Soothing Tears
- Size: 0.5 fl oz (15 mL)
- Lot Codes & Expiration Dates:
SY24K01 / SY24K02 – 09/30/2026
- Product Quantity: 74,016 bottles
- Brands include Rugby and Walgreens
- Lubricating formula
PRODUCT: Artificial Tears Sterile Lubricant Eye Drops
- Size: 0.5 fl oz (15 mL)
- Lot Codes & Expiration Dates:
AT24D01 – 04/30/2026
AT24E01 / AT24E02 – 05/31/2026
AT24G01 – 07/31/2026
- Product Quantity: 589,848 bottles
- Multiple brands (e.g., Leader, Kroger, Publix, TopCare, etc.)
- Artificial tears formulation
The issue was discovered through internal testing, leading to the recall's initiation on March 3, 2026. The recall is classified as Class II, indicating a potential health risk. The classification date was March 31, 2026.
Source: www.accessdata.fda.gov/scripts/ires/
27
Comentários
Comentário